Учебник БИОЛОГИЯ 10—11 классы - Общие закономерности - А.А. Вахрушев - Баласс 2015 год
Белки и нуклеиновые кислоты - строительный материал и источник энергии клетки - КЛЕТКА КАК СТРУКТУРНАЯ ЕДИНИЦА ОРГАНИЗМА
Постановка проблемы урока
Обыватель:Разве можно информацию о свойствах всего организма поместить в каждую клетку?
Биолог:Так оно и есть: в каждой клетке находятся молекулы, в которых “зашифрованы” все свойства организма. Вопрос в том, как организовать хранение и использование этой информации.
• В чём противоречие? На какой вопрос мы будем искать ответ? Предложите свой и сравните с вариантом авторов на с. 396.
Необходимые базовые знания
• Что такое наследственная информация? (9 класс)
• Что такое заменимые и незаменимые аминокислоты? (9 класс)
• Вспомните, какие белки участвуют в транспорте кислорода по телу, в пищеварении, регуляции функций организма и т.д. (8, 9 класс)
• Откуда живые организмы получают энергию? (9 класс)
Решение проблемы
Белки: строение и уровни структуры
• Какие уровни структуры имеет молекула белка?
Полимерные макромолекулы белков построены из небольших мономеров —аминокислот.Как следует из их названия, все аминокислоты имеют аминогруппу NН2и карбоксильную (кислотную) группу СООН. Между ними располагается радикал (некая группа атомов -R), отличающий аминокислоту каждого вида от всех других. Среди радикалов - основные, кислотные, спиртовые (ОН) или тиоловые (SН) группы и некоторые их комбинации, различные углеводороды.
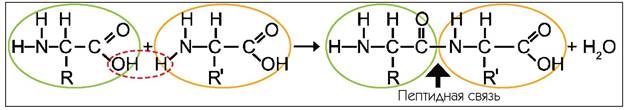
Аминокислот, участвующих в построении большинства белков, всего 20 видов. Ковалентная связь, образуемая в результате химической реакции между аминогруппой одной аминокислоты и карбоксильной группой другой (с выделением одной молекулы воды, без участия радикала), называется пептидной связью. Аминокислотные остатки, т.е. аминокислоты, израсходовавшие аминогруппу и (или) карбоксильную группу, скреплены этими связями в длинные неветвящиеся цепочки — полипептиды. Наиболее часто встречающиеся полипептиды могут состоять из нескольких сотен, а иногда и тысяч аминокислотных остатков.
Соединяясь в различной последовательности, аминокислоты образовали бы бесконечное множество сочетаний, но только немногие случайные комбинации могли бы оказаться функциональными в организме. Например, далеко не все сочетания букв образуют осмысленные слова в каждом языке. К счастью, аминокислотные остатки в живой клетке соединяются в строго определённом порядке, что и определяет их функциональные свойства. Этот порядок — последовательность аминокислотных остатков в полипептидной цепи — называетсяпервичной структурой белка.
8.1. Схема образования пептидной связи
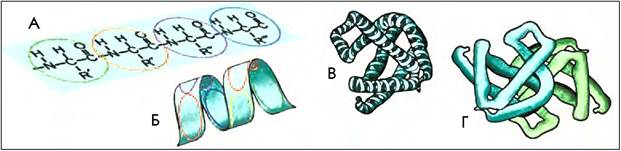
Участки полипептидной цепи, в зависимости от расположения радикалов на аминокислотных остатках, изгибаются, принимают заданную форму и скрепляются водородными связями между NН- и СО-группами пептидного остова. Одни участки свиваются в спираль (рис. 8.2) или образуют складчатые слои, имеющие вид “гармошек”. Другие участки плавно изгибаются или сохраняют линейную форму. Всё это — элементывторичной структурыбелковой молекулы. Она определяется первичной структурой.
Боковые радикалы некоторых аминокислот полярны: они несут на себе частичные заряды. Эти радикалы взаимодействуют друг с другом и с молекулами воды. В то же время гидрофобные (т.е. “стремящиеся прочь от воды”) радикалы группируются вместе с себе подобными, образуя “гидрофобное ядро” внутри белковой молекулы. Если же гидрофобные радикалы окажутся снаружи, то такой белок будет избегать контактов с водой и “прятаться” среди других молекул, например, в клеточных мембранах. В итоге из элементов вторичной структуры формируются более крупные части (субъединицы) белковой молекулы: глобулы (комочки), фибриллы (волокна). Они составляюттретичную структуру.
Многие зрелые белки состоят из нескольких субъединиц. Их укладка в пространстве называетсячетвертичной структурой.
8.2. Строение белковой молекулы: А - первичная структура; Б — вторичная; В ~ третичная; Г — четвертичная
Свойства белков
• Как свойства белка связаны с его структурой?
Сложная пространственная организация молекулы белка позволяет ей распознавать и связывать только определённые молекулы. Молекулы должны подходить друг другу, как ключ к замку.
Функция белка, таким образом, полностью зависит от формы молекулы. Эта уникальная форма определяется первичной структурой, значит, последовательность соединения аминокислот содержит полную информацию не только о структуре, но также и о функциях белка. Образно говоря, такая “информационная” молекула содержит в себе инструкцию по самосборке и всем дальнейшим действиям. Совместные действия различных белков обеспечивают обмен веществ — то, что, собственно, и называется жизнью.
Замена даже одной аминокислоты может привести к весьма значительным изменениям свойств белковой молекулы, в то время как замены многих других аминокислот могут не оказать существенного влияния на её функции.
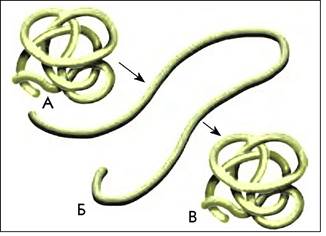
Так как заряд радикалов на боках аминокислотной цепочки зависит от кислотности среды (рН), воздействие на белок кислотой приводит к нарушению сложной структуры молекулы. Цепь разворачивается несмотря на то, что последовательность аминокислот не нарушена. Этот процесс называетсяденатурацией.Денатурацию молочного белка казеина мы наблюдаем при скисании молока. Молоко сворачивается, так как рвутся нековалентные связи, стабилизирующие нормальную структуру казеина, и он становится нерастворимым. Денатурация может быть вызвана и другими факторами, например, нагреванием. Если фактор, вызвавший денатурацию белка, не был слишком жёстким, при прекращении его воздействия белок может восстановить свою структуру. Обратимая денатурация белков лежит в основе большинства обратимых функций организма, например, утомляемости мышц, раздражимости.
8.3. Обратимая денатурация белков:А — молекула до денатурации; Б — денатурированный белок; В - восстановленная молекула
Белки выполняют разнообразные функции. Некоторые белки служат строительным материалом клетки, но большинство — ускоряют протекание химических реакций (и даже управляют их последовательностью), т.е. являются биологическими катализаторами, илиферментами.В конечном счёте белки обусловливают всё разнообразие свойств живых организмов.
8.4. Биологические функции белков
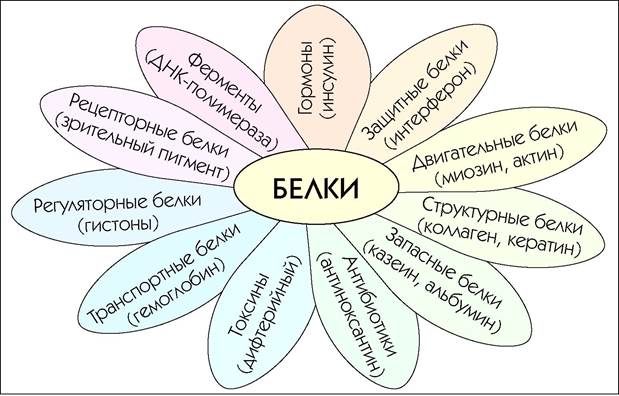
Ферменты
• Каким образом фермент обеспечивает протекание биохимической реакции?
Ферменты— это биологические катализаторы, которые ускоряют химические реакции в тысячи раз. Каждый фермент катализирует определённую реакцию, поэтому даже в отдельной клетке содержатся сотни различных ферментов — столько, сколько требуется для обеспечения всех протекающих в ней процессов.
Чтобы крупные органические молекулы вступили в реакцию друг с другом, необходимо, чтобы функциональные группы этих молекул были обращены друг к другу и никакие другие молекулы не мешали их взаимодействию. Вероятность того, что молекулы сами сориентируются нужным образом, ничтожно мала. Фермент же присоединяет к себе обе молекулы в нужном положении, снижает порог энергии, необходимой для начала реакции, и освобождает готовый продукт. Таким образом, фермент создаёт “режим наибольшего благоприятствования” для прохождения конкретной реакции.
Уникальная трёхмерная структура молекулы фермента не только позволяет соединять исходные продукты реакции и освобождать конечные. В определённом месте молекулы, как правило, имеется активный центр, где расположены аминокислотные радикалы, непосредственно участвующие в катализе. Подобно другим химическим катализаторам, они изменяются в ходе реакции, но мгновенно восстанавливаются. Например, фермент отдаёт свой ион водорода одному реагенту, но тут же получает взамен другой от следующего реагента. Так, фермент выполняет свою работу снова и снова, как станок на конвейере.
Ферменты — это совершенные “молекулярные машины”, без которых невозможно представить существование клеточных живых форм. Полагают, что древнейшие ферменты на заре зарождения жизни на Земле состояли из РНК, а белки появились позже.
Нуклеиновые кислоты
• Из каких мономеров построены нуклеиновые кислоты?
Как и белки,нуклеиновые кислотыотличаются от других органических веществ тем, что в них строго определённая последовательность мономерных звеньев. Строительными блоками — мономерами — для огромных молекул нуклеиновых кислот служат нуклеотиды.
В отличие от аминокислот, нуклеотиды очень сходны по своим химическим свойствам и строению. Молекула нуклеотида состоит из трёх элементов: пятиуглеродного сахара, азотистого основания и остатка фосфорной кислоты. В зависимости от сахара в составе нуклеотидов различают два типа нуклеиновых кислот. Рибонуклеиновые кислоты (РНК) содержат сахар рибозу, а дезоксирибонуклеиновые (ДНК) - дезоксирибозу. В составе нуклеотида может быть одно из пяти азотистых оснований (их обозначают по первым буквам). В их число входят два относительно крупных пурина: аденин (А) и гуанин (Г) и три мелких пиримидина: цитозин (Ц), тимин (Т) и урацил (У). В состав ДНК входят А, Г, Ц и Т, а в состав РНК - А, Г, Ц и У.
8.5. Структура нуклеида - мономера ДНК
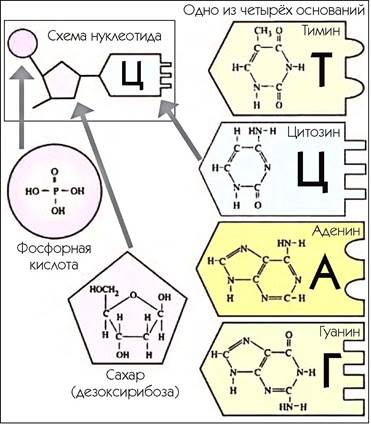
Сахара, связываясь фосфатными группами, образуют сахарофосфатный остов, на которой, как бусины, “нанизаны” азотистые основания.
![]() Сахарофосфатный остов и, следовательно, цепи ДНК и РНК полярны, т.е. имеют начало и конец. Их соответственно обозначают 5' (пять-штрих) и 3' (три-штрих) - по номеру атома углерода пентозы терминального нуклеотида, не занятого связью с предыдущим или последующим нуклеотидом.
Сахарофосфатный остов и, следовательно, цепи ДНК и РНК полярны, т.е. имеют начало и конец. Их соответственно обозначают 5' (пять-штрих) и 3' (три-штрих) - по номеру атома углерода пентозы терминального нуклеотида, не занятого связью с предыдущим или последующим нуклеотидом.
Таким образом, 3'-конец рибонуклеиновой кислоты содержит свободную ОН-группу пентозы, к которой может присоединиться фосфат следующего нуклеотида.
Структура и функции ДНК
Как происходит кодирование и хранение наследственной информации?
В 1953 году Джеймс Уотсон и Френсис Крик установили структуру нуклеиновых кислот и их значение в передаче наследственной информации. Молекула ДНК состоит из двух цепочек нуклеотидов. Между двумя цепочками располагается “лесенка” из азотистых оснований, сшитых в поперечном направлении слабыми водородными связями. Так как азотистые основания различаются размером и числом возможных водородных связей, друг против друга в этой “лесенке” могут разместиться только комплементарные (взаимно дополняющие) парыA=Ти Г=Ц.Двойная цепь ДНК закручена в спираль.
8.6. Структура ДНК
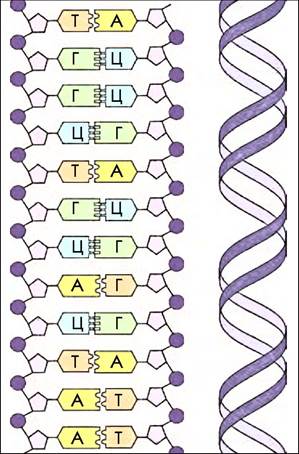
ДНК служит хранилищем информации о строении организма. Её копии передаются от родительской клетки к дочерним и от родительского организма к его потомкам по наследству. Информация закодированапоследовательностью азотистых основанийв одной из цепей ДНК - смысловой. Другая цепь ДНК — защитная. Она состоит из комплементарных нуклеотидов и закрывает доступ к считыванию информации. Вместе с тем защитная цепь является “зеркальным отражением” смысловой. Поэтому по одной цепи можно полностью восстановить структуру другой. Это свойство комплементарных цепей активно используется в клетке для удвоения (репликации) ДНК и для “починки” (репарации) отдельных участков в случае повреждения.
Структура и функции РНК
• Как происходит считывание и использование наследственной информации?
ДНК обеспечивает лишь хранение и наследование информации. Чтобы эту информацию использовать, необходимы РНК — нуклеиновые кислоты иного типа. Их состав отличается тем, что содержит другой сахар (рибозу) и другой набор оснований (урацил вместо тимина). Главное же отличие в том, что РНК состоит только из одной цепочки. Молекула РНК собирается на смысловой цепи ДНК путём подстановки комплементарных нуклеотидов. Чтобы это было возможным, специальный фермент обеспечивает к ней доступ, “расстёгивая” связи между двумя её цепочками. Сборка РНК - это безошибочное переписывание (транскрипция) некоторой части информации с ДНК на РНК языком последовательности её нуклеотидов. Затем РНК переносит рабочую инструкцию в другие части клетки.
Существует несколько типов РНК, функции которых различны. Информационная РНК, или иРНК (иначе — матричная, мРНК), несёт инструкцию о первичной структуре молекулы какого-либо белка. Транспортные РНК (тРНК) содержат нуклеотидный код определённой аминокислоты и способны доставлять их в место сборки молекулы белка. Рибосомная РНК (рРНК) входит в состав рибосом, определяет их структуру и управляет их функцией — синтезом белка по инструкции.
![]() В последние годы были открыты новые виды РНК, которые выполняют важные регуляторные и защитные функции. РНК является наследственным материалом многих вирусов. В их числе вирусы гриппа и иммунодефицита,полиовирус, вирус бешенства и т.д. Считают, что до появления клеток современного типа на Земле господствовал “мир РНК” - без ДНК и белков, которые возникли позднее.
В последние годы были открыты новые виды РНК, которые выполняют важные регуляторные и защитные функции. РНК является наследственным материалом многих вирусов. В их числе вирусы гриппа и иммунодефицита,полиовирус, вирус бешенства и т.д. Считают, что до появления клеток современного типа на Земле господствовал “мир РНК” - без ДНК и белков, которые возникли позднее.
Итак, информация, записанная в ДНК, переписывается на иРНК в виде отдельных инструкций и доставляется в рабочие участки клетки. Другие виды РНК запускают синтез основных “исполнителей” инструкций — белков с такой последовательностью аминокислот, которая указана в инструкции языком последовательности нуклеотидов. Так происходит трансляция - перевод информации с языка нуклеотидного кода на язык последовательности аминокислот белка. Эта последовательность, как мы знаем, определяет структуру и функции белка. Совместные действия всех белков и РНК обеспечивают жизнедеятельность каждой клетки и организма в целом.
Молекулы - переносчики энергии
• Как энергия пищи становится доступной для использования в жизненных процессах?
Рольнуклеотидов не ограничивается тем, что они служат строительными блоками нуклеиновых кислот. Некоторые нуклеотиды являются основой других активных веществ клетки. Важнейшие из них — переносчики энергии: АТФ (аденозинтрифосфат), НАДФ (никотинамидаде- ниндинуклеотидфосфат) и др.
Для поддержания жизнедеятельности клетки в неё постоянно поступает энергия, которая запасается в форме химических связей органических молекул. Самый распространённый молекулярный аккумулятор —аденозинтрифосфат (АТФ).В молекуле этого вещества азотистое основание присоединено к молекуле сахара рибозе, а к ней крепится “хвост” из трёх неорганических фосфатов. Именно в связях между фосфатами АТФ запасается энергия.
Когда один (или два) фосфат(а) АТФ отщепляется, выделяется большое количество энергии, которое клетка использует в своей жизнедеятельности. Такие связи называютвысокоэнергетическими,или макроэргическими, связями.
Все химические реакции в организме, обеспечивающие приток энергии извне (фотосинтез, расщепление пищи), в конечном счёте ведут к синтезу АТФ, а процессы жизнедеятельности — к расходованию этого заряда энергии. Энергия используется, например, при синтезе биологических молекул, активном транспорте через клеточные мембраны, движении клеток и т. д.
8.8. Строение молекулы аденозинтрифосфата(АТФ)
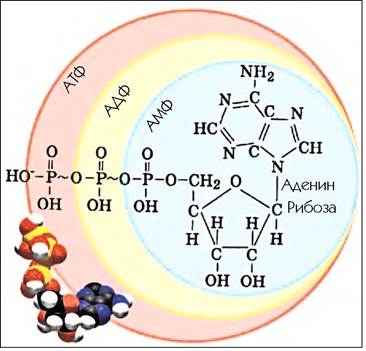
Обобщение новых знаний
Бедки и нуклеиновые кислоты представляют собой макромолекулы, построенные из большого числа мономеров, соединённых в определённую последовательность, от которой зависят их свойства. С помощью РНК эта информация в виде отдельных инструкций воплощается в синтезе белков с определённой последовательностью аминокислот. Последовательность аминокислот, в свою очередь, определяет порядок скручивания и складывания белка в молекулу определённой формы. Белки-ферменты предназначены для управления биохимическими реакциями, составляющими основу всех процессов жизнедеятельности клетки. Молекулы АТф обеспечивают доставку энергии в место её использования.
Белки, аминокислоты, ферменты. Нуклеотиды, ДНК, РНК, АТФ
Применение знаний
1. Как построена молекула белка?
2. Каким образом первичная структура белка определяет его окончательную форму и функции?
3. Перечислите характерные свойства ферментов.
4. Почему белки и нуклеиновые кислоты называют “информационными молекулами”?
5. Каковы функции белков в организме?
6. Как хранится и используется наследственная информация?
7. Какая особенность молекулы АТФ позволяет ей запасать энергию?
8. Одна из цепочек ДНК имеет такую последовательность нуклеотидов: АГТАЦЦГАТАЦТЦГАТТТАЦГ. Какую последовательность нуклеотидов имеет вторая цепочка той же молекулы?
9. Как происходит наследственная передача свойств белка от родительской клетки к дочерней?
10. Почему контролируемые ферментами реакции зависят от температуры, рН и т.д.?
Мои биологические исследования
Расщепление пироксида водорода живыми клетками как проявление ферментативной функции белков
Пероксид водорода - токсичный продукт обмена веществ клетки, который расщепляется на кислород и воду. Приготовьте 3%-ный раствор пироксида водорода и капните несколько капель раствора на кусочки сырого и варёного картофеля. Объясните получившиеся результаты.