Настольная книга учителя химии 10 класс - поурочные разработки
ВАЖНЕЙШИЕ МОНОСАХАРИДЫ, ИХ СТРОЕНИЕ И СВОЙСТВА - УГЛЕВОДЫ
Цели урока. Познакомить учащихся с важнейшими представителями моносахаридов, их строением и отображением этого строения на письме с помощью формул Фишера и Жуарса. Дать понятие о таутомерии. Рассмотреть альдегидные и спиртовые свойства глюкозы, а также реакции брожения ее.
Оборудование: глюкоза, NaHCО3, растворы CuSО4, NaOH. Демонстрационные образцы: прозрачные фруктовые соки (свежие или консервированные), мёд. Химический стакан (250 мл), настольная лампа, аквариумная водоросль (лучше — элодея).
I. Общее строение моносахаридов
Итак, ребятам уже известен первичный набор сведений: углеводы содержат в составе молекулы альдегидный (или кетонный) фрагмент и несколько гидроксильных групп. Их состав в большинстве случаев соответствует общей формуле Сn(Н2О)m.
Простейшим моносахаридом можно считать глицериновый альдегид, имеющий формулу НОСН2—СНОН—СНО. Учитель задает классу вопрос: имеет ли это вещество оптические изомеры? Центральный углеродный атом глицеринового альдегида связан с четырьмя различными заместителями и, следовательно, является асимметрическим центром. Для таких веществ возможно существование двух оптических изомеров. Как же их изобразить на плоскости? Это удобно делать с помощью проекционных формул Фишера. Цепочку моносахарида мысленно берут «за голову» (карбонильный атом углерода), поднимают вертикально, кладут на лист бумаги (вдоль длинной стороны) и «прокатывают асфальтовым катком». Молекула «расплющивается», причем, для различных оптических изомеров гидроксильные группы при асимметрическом центре будут располагаться по разные стороны углеродной цепи. Углеродная цепочка нумеруется, начиная с верхнего атома. Формулы двух оптических изомеров глицеринового альдегида выглядят следующим образом:

Тот изомер, у которого гидроксильная группа расположена справа от основной цепи, называют D-глицериновый альдегид (от латинского dexter — правый), второй — соответственно L-глицериновый альдегид (laevus — левый). Кроме глицеринового альдегида, других триоз-сахаров нет. Далее в ряду углеводов следуют тетрозы. У них появляется еще один фрагмент Н—С—ОН и новый асимметрический центр.
Формулы Фишера наглядно показывают взаимное расположение атомов водорода и гидроксильных групп при таких центрах. По положению заместителей при наиболее удаленном от карбонильной группы асимметрическом углероде все моносахариды относят к D или L-ряду в соответствии с конфигурацией D и L-глицеринового альдегида. Изменение конфигурации у любого иного асимметрического центра соответствует уже другому углеводу. Следует отметить, что в природе обнаружены моносахариды только D-ряда. Учитель демонстрирует ребятам плакат, на котором изображены некоторые представители тетроз, пентоз и гексоз. Все они относятся к D-ряру. Теперь учитель имеет возможность вернуться к схеме классификации углеводов (см. рис. 33) и найти среди приведенных формул альдозы и кетоза; тетрозы, пентозы и гексозы. Учитель также обращает внимание на то, чем дезоксиуглевод отличается от обычного моносахарида.
Конечно, учащихся смущает такое обилие новых названий и формул. Успокойте ребят. Во-первых, если при написании уравнения реакции не требуется детальная расшифровка структуры углевода, их формулы изображают в упрощенном виде. Во-вторых, не все из приведенных углеводов необходимо знать даже в профильном классе (далее пригодятся только рибоза с дезоксирибозой, глюкоза и фруктоза). В-третьих, формулы важнейших моносахаридов можно выписать на карточку-подсказку.
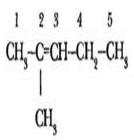
II. Глюкоза, ее строение и свойства
Глюкоза представляет собой наиболее распространенный и, безусловно, наиболее важный моносахарид. Она содержится в соке винограда (отсюда еще одно название глюкозы — виноградный сахар), других ягод и фруктов, является структурным звеном сахарозы, клетчатки и крахмала. В крови человека содержится около 0,1% D-глюкозы.
Строение молекулы и физические свойства. Учитель вновь обращается к плакату с изображением важнейших моносахаридов. Молекулярная формула глюкозы C6H12О6. Она имеет неразветвленный углеродный скелет и представляет собой альдегидоспирт, содержащий одну альдегидную и пять гидроксильных групп. Внешний вид глюкозы ребятам уже знаком: белые игольчатые кристаллы сладкого вкуса, хорошо растворимы в воде.
Методически наиболее сложным для объяснения является вопрос кольчато-цепной таутомерии глюкозы. Учитель может воспользоваться кодограммой или плакатом, изображенным на рисунке 34. Комментарий к рисунку может быть примерно таким. Благодаря свободному вращению углеродной цепочки относительно простых С—С связей, в водном растворе альдегидная группа оказывается сближена с гидроксилом при 5-м углеродном атоме. Эти функциональные группы сильно полярны, поэтому гидроксил сравнительно легко присоединяется по двойной связи карбонильной группы. В результате такого внутримолекулярного присоединения образуются две возможные циклические формы глюкозы. Они представляют собой шестичленный цикл, содержащий атом кислорода. В циклических формах глюкозы по-прежнему пять гидроксильных групп, однако гидроксил при С(1), образованный из альдегидной группы цепной формы, имеет особые свойства и называется гликозидным гидроксилом.
Рис. 34. Превращение цепной формы глюкозы в циклические α- и β-формы
Циклические формы углеводов удобно изображать перспективными формулами Хеуорса. Цикл условно считают плоским и проектируют на плоскость листа под некоторым утлом, причем атом кислорода изображают на максимальном удалении справа. Ближняя часть кольца на рисунке изображается снизу и иногда выделяется более жирной линией.
Циклические формы глюкозы различаются взаимным положением гликозидного гидроксила и гидроксильной группы при последнем углеродном атоме С(6). Если эти группы находятся по разные стороны цикла, такой изомер называют a-D-глюкоза, если по одну сторону— β-D-глюкоза (или просто α- или β-глюкоза). В водном растворе присутствуют в равновесии все три формы глюкозы: цепная (в очень незначительном количестве) и обе циклические. В твердом состоянии глюкоза может существовать в одной из двух циклических форм.
Учитель должен быть готов просто и понятно ответить на вопросы, которые обязательно зададут любознательные ребята. А может быть, даже предупредить эти вопросы.
1. Почему группа —СН2ОН изображена над циклом? Это определяется оптической изомерией углевода. Для D-изомеров шестой атом углерода в формуле Хеуорса всегда будет располагаться над плоскостью цикла, для L-изомеров — под ней.
2. Как запомнить, где располагать гидроксильные группы при 2, 3 и 4-х атомах углерода? Это можно легко сделать, имея перед глазами формулу Фишера. Атомы или группы атомов, изображаемые в формулах Фишера справа, в формулах Хеуорса располагаются под плоскостью цикла и наоборот (вот вам и польза карточки-подсказки). Для глюкозы, как самого важного углевода, желательно писать гидроксилы при С(2), С(3) и С(4) машинально: под-над-под.
3. Как запомнить расположение гликозидного гидроксила для α и β-изомеров глюкозы? Нет ничего проще: расположение — ОН сверху или снизу определяется самим начертанием букв α- и β-. Сравните: «головка снизу» и «головка сверху».

Получение глюкозы. Из курса биологии ребята знают, что глюкоза образуется в зеленых листьях растений из углекислого газа, поглощаемого из воздуха, и воды под действием солнечного света. Этот процесс протекает только в присутствии особого вещества — хлоролла — и называется фотосинтезом. Химические реакции, протекающие при этом, чрезвычайно сложны. Упрощенно фотосинтез можно изобразить уравнением:
![]()
Роль фотосинтеза на Земле трудно переоценить. Это единственный источник кислорода в атмосфере нашей планеты и органического углерода всей живой природы. За счет фотосинтеза происходит связывание углекислого газа, что исключает его накопление в воздухе. Фотосинтез обеспечивает превращение световой энергии в химическую, которая затем в живых организмах способна превращаться в другие виды энергии. В промышленности глюкозу получают гидролизом крахмала или целлюлозы, о чем речь пойдет на последующих уроках.
Можно ли увидеть процесс фотосинтеза? Оказывается, нет ничего проще! В химический стакан объемом 250 см3 с дистиллированной водой учитель помещает аквариумную водоросль (желательно — элодею) и добавляет щепотку гидрокарбоната натрия (за счет гидролиза он увеличивает содержание растворенного СО2 в воде). Стакан устанавливают на демонстрационный столик и освещают светом настольной лампы (рис. 35). Через несколько минут будет заметно выделение пузырьков газа, поднимающихся на поверхность воды. Это кислород.
Рис. 35. Демонстрация образования кислорода в процессе фотосинтеза
Химические свойства. Глюкоза как представитель полиоксиальдегидов проявляет свойства многоатомных спиртов и свойства альдегидов, а также имеет ряд специфических особенностей.
1. Реакции по альдегидной группе. Как альдегид глюкоза легко окисляется, восстанавливается, присоединяет цианистый водород, дает продукты конденсации. Однако она не взаимодействует с раствором гидросульфита натрия.
1) Глюкоза является восстанавливающим моносахаридом и окисляется при нагревании реактивами Толенса (реакция «серебряного зеркала») и Фелинга (гидроксид меди (II) в щелочной среде):

Образующееся соединение называется глюконовой кислотой.
Реакцию «серебряного зеркала» на чистой глюкозе ребята уже видели. Поэтому целесообразно испытать на наличие глюкозы реальные объекты с помощью гидроксида меди (II). В несколько пробирок учитель наливает по 1 мл раствора NaOH, добавляет 2-3 капли раствора медного купороса и несколько капель фруктового или ягодного сока, экстракт изюминки, сока свежего огурца, раствор мёда, варенья и др. Осадок гидроксида меди (II) сначала растворяется, затем при нагревании раствор приобретает окраску от красной до желто-оранжевой. Это свидетельствует о наличии в исследуемых жидкостях виноградного сахара — глюкозы.
2) Более сильный окислитель — азотная кислота — окисляет не только альдегидную группу, но и 6-й углеродный атом до карбоксила. Образующаяся двухосновная кислота называется сахарной:
![]()
3) При восстановлении альдегидной группы глюкозы образуется шестиатомный спирт сорбит:
![]()
4) Присоединение синильной кислоты. Подобно алифатическим альдегидам, глюкоза присоединяет молекулу синильной кислоты, что позволяет увеличивать длину цепи углеводов:
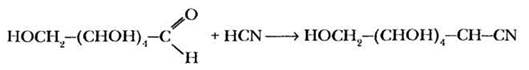
2. Реакции гидроксильных групп. Глюкоза проявляет свойства многоатомных спиртов. Одна из гидроксильных групп циклической формы, а именно гликозидный гидроксил имеет особые свойства.
1) Образование простых эфиров. При действии йодистого метила атом водорода во всех гидроксильных группах замещается на метальный радикал:
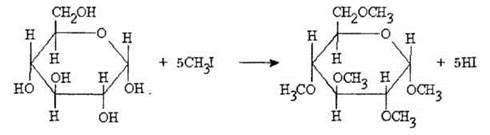
2) Образование глюкозидов. При действии метилового спирта в кислой среде простой эфир образуется только за счет гликозидного гидроксила циклической формы:
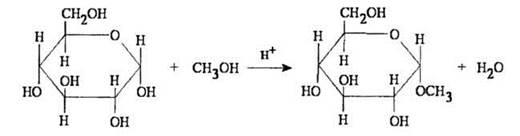
Продукты замещения водородного атома гликозидной гидроксильной группы называются в общем случае гликозидами, а конкретно для глюкозы — глюкозидами. В приведенном примере образуется α-D-метилглюкозид. Это соединение уже не способно к образованию цепной (открытой) формы, поскольку не содержит ответственного за это гликозидного гидроксила.
3) Образование сложных эфиров. Под действием уксусного ангидрида гидроксильные группы глюкозы вступают в реакцию этерификации:
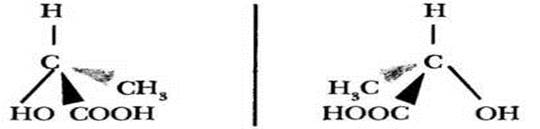
4) Образование алкоголятов. Свежеприготовленный осадок гидроксида меди (II) реагирует с раствором глюкозы с образованием растворимой в воде комплексной соли ярко-синего цвета:
Подобные алкоголяты, образованные углеводами, называются общим термином сахараты.
3. Специфические свойства глюкозы.
1) Под действием микроорганизмов или ферментов глюкоза способна расщепляться с образованием молекул с меньшей молекулярной массой. Этот процесс называется брожением. Существует несколько типов брожения, важнейшими из которых являются спиртовое, молочно-кислое и масляно-кислое:
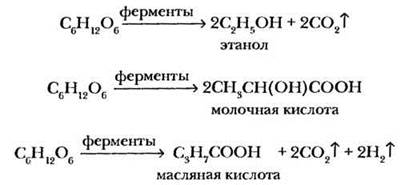
2) В живом организме происходит окисление глюкозы кислородом воздуха, в результате которого образуется углекислый газ и выделяется большое количество энергии, необходимой для функционирования клетки. Таким образом, глюкоза является своеобразным аккумулятором солнечной энергии.
![]()
III. Краткие сведения о других моносахаридах
1. Фруктоза
Наиболее важная из кетоз — D-фруктоза. Она широко распространена в растительном мире: содержится во фруктах, в пчелином мёде, входит в состав дисахарида сахарозы.
Структура и физические свойства. Учитель вновь проецирует на экран кодограмму с формулами важнейших моносахаридов. Фруктоза изомерна глюкозе и имеет молекулярную формулу С6Н12О6. Она представляет собой кетогексозу с карбонильной группой у второго углеродного атома цепи. Фруктоза, как и глюкоза, способна существовать в открытой и двух циклических формах. Особенностью ее циклических форм является меньший размер цикла, содержащего не шесть, а пять атомов. Равновесные формы фруктозы представлены на рисунке 36. Наиболее подготовленные учащиеся на примере фруктозы и последующих рибозы и дезоксирибозы отрабатывают превращение проекционных формул Фишера в перспективные Хеуорса.
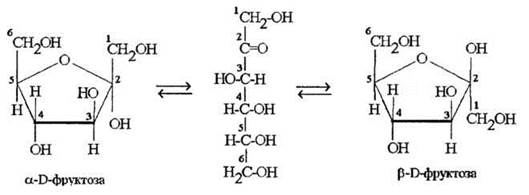
Рис. 36. Цепная и циклические формы D-фруктозы
Фруктоза — белые кристаллы, хорошо растворимые в воде. Она имеет более сладкий вкус, чем глюкоза и сахароза.
Химические свойства. Фруктоза вступает во все реакции многоатомных спиртов: образует сахараты с нерастворимыми в воде гидроксидами, простые и сложные эфиры. Однако наличие в молекуле вместо альдегидной группы кетонного фрагмента затрудняет реакции окисления фруктозы. Например, глюкоза окисляется бромной водой до глюконовой кислоты, а фруктоза к подобному превращению не способна. Эта реакция позволяет отличить альдозы от кетоз.
Как и все моносахариды, фруктоза не подвергается гидролизу.
2. Рибоза и дезоксирибоза
В качестве представителей альдопентоз, играющих важнейшую роль для живых организмов, в классах с углубленным изучением химии учитель приводит D-рибозу и D-дезоксирибозу. Молекулярная формула рибозы C5H10O5, она содержит альдегидную и четыре гидроксильные группы. Дезоксирибоза не имеет при втором углеродном атоме гидроксильной группы, ее составC5H10O4. Несмотря на то что формально эта молекула не отвечает формуле Cn(H2O)m, по химической сущности и биологической функции дезоксирибозу также относят к углеводам.
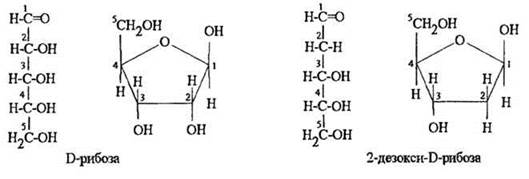
Рибоза и дезоксирибоза в виде N-гликозидов с пуриновыми и пиримидиновыми основаниями входит в состав нуклеиновых кислот (ДНК и РНК).
Задание 1
1-й уровень
В двух пробирках без этикеток находятся растворы глюкозы и этиленгликоля. С помощью каких химических реакций можно различить эти вещества?
2-й уровень
Как при помощи одного реактива распознать растворы следующих веществ: уксусная кислота, пропаналь, глюкоза, глицерин, метанол? Напишите уравнения соответствующих реакций.
Задание 2
1-й уровень
Требуется получить 2000 г 2%-ного раствора фруктозы из 10%-ного. Какой объем воды и какую массу 10%-ного раствора необходимо взять для этого?
2-й уровень
Смешали 100 г 10%-ного и 200 г 5%-ного растворов глюкозы. Какова массовая доля углевода в полученном растворе?
Задание 3
1-й уровень
При сжигании 45 г глюкозы выделилось 704 кДж теплоты. Составьте термохимическое уравнение этой реакции.
2-й уровень
Процесс фотосинтеза можно условно представить следующим уравнением:
![]()
Каждый квадратный сантиметр земной поверхности ежеминутно получает в среднем 2 Дж солнечной энергии. Сколько времени потребуется, чтобы в 10 листьях образовалась глюкоза массой 0,9 г, если площадь каждого листа 10 см2, а солнечная энергия используется только на 10%?