Диагностические работы химия 9 класс - 2017 год
ВАРИАНТ 6
Часть 1
Для выполнения заданий 1-15 в поле ответа запишите одну цифру, которая соответствует номеру правильного ответа.
1. Элемент, в атоме которого содержится такое же число энергетических уровней, что и в атоме Na, это:
1) С1
2) Li
3) Be
4) К
![]()
2. Ряд химических элементов, в котором уменьшаются неметаллические свойства, это:
1) Li, Be, В
2) S, Р, Si
3) Са, Mg, Be
4) Br, Cl, F
![]()
3. В азотной кислоте химическая связь:
1) только ионная
2) только ковалентная полярная
3) ионная и ковалентная неполярная
4) ионная и ковалентная полярная
![]()
4. Степени окисления хлора в веществах АlСl3 и Са(ОСl)2 соответственно равны:
1) -1 и + 2
2) +3 и +5
3) +1 и + 1
4) -1 и + 1
![]()
5. Только соли находятся в ряду:
1) NaNO3, H2SiO3, СаСO3
2) BaSO4, SO3, KNO3
3) NH4NO3, NaHCO3, KCl
4) AlCl3, HCl, Na2O
![]()
6. Соответствует уравнению реакции соединения запись:
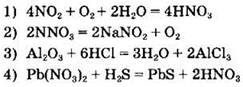
![]()
7. Минимальное число ионов образуется при диссоциации 1 моль вещества:
1) сульфата калия
2) хлорида алюминия
3) соляной кислоты
4) плавиковой кислоты
![]()
8. Сокращенному ионному уравнению Cu2+ + 2OН- = Сu(ОН)2 соответствует молекулярное уравнение реакции между веществами:
1) Н2O и CuSO4
2) CU(NO3)2 + NaOH
3) CuO + H2O
4) CuSO4 + Mg(OH)2
![]()
9. Алюминий реагирует со всеми веществами в ряду:
1) O2, СаСO3, Н2O
2) Cl2, НСl, KNO3
3) HBr, NaOH, Fe3O4
4) BaO, O2, HNO3
![]()
10. Соляная кислота реагирует с каждым из двух веществ:
1) Na2SO4 и CaO
2) ZnO и NO
3) Ag и СаО
4) Ва(ОН)2 и Zn
![]()
11. Реакция возможна между веществами:
1) Cu + AgCl
2) AgNO3 + НСl
3) H2SiO3 + Fe(NO3)2
4) CaO + NaOH
![]()
12. И с оксидом фосфора и с серной кислотой реагирует вещество:
1) нитрат бария
2) вода
3) гидроксид железа (III)
4) гидроксид бария
![]()
13. Верны ли утверждения о свойствах веществ: А) водород образует взрывчатые смеси с кислородом; Б) хлор — ядовитое вещество:
1) верно только А
2) верно только Б
3) верны оба утверждения
4) оба утверждения неверны
![]()
14. В реакции, схема которой ![]() окислителем является:
окислителем является:
1) Сu+2
2) N+5
3) О2
4) N+4
![]()
15. Массовые доли элементов в сульфате железа (III) равны:
1) Fe — 28%, О — 48%
2) S — 24%, О — 42,1%
3) Fe — 36,9%, S — 21%
4) S — 21%, О — 28%
![]()
При выполнении заданий Ns 16, 17 из предложенного перечня ответов выберите два правильных и запишите в таблицу цифры, под которыми они указаны.
16. Для серы и хлора верными являются утверждения:
1) атомы элементов содержат одинаковое число электронов на внешнем энергетическом уровне
2) образуют простые вещества — неметаллы
3) электроотрицательность элементов меньше, чем у фтора
4) имеют степень окисления -2
5) имеют одинаковый радиус атома
Ответ: ![]()
17. Для метана и этилена верны следующие утверждения:
1) вещества содержат 2 атома углерода
2) в молекулах веществ присутствуют только одинарные связи
3) вещества практически не растворимы в воде
4) вещества присоединяют водород
5) вещества горят в кислороде
Ответ: ![]()
При выполнении заданий № 16 и 19 к каждому элементу первого столбца подберите соответствующий элемент из второго столбца. Запишите в таблицы выбранные цифры под соответствующими буквами. Цифры в ответах могут повторяться.
18. Установите соответствие между двумя веществами и реактивом, с помощью которого можно различить эти вещества.
|
ВЕЩЕСТВА |
РЕАКТИВ |
|
А) НСl и NaOH |
1) NaOH |
|
Б) СuСl2 и КСl |
2) H2SO4 |
|
В) Na2CO3 и Na2SiO3 |
3) Аl(ОН)3 |
|
4) фенолфталеин |
Ответ: ![]()
19. Установите соответствие между названием вещества и реагентами, с которыми это вещество может взаимодействовать.
|
НАЗВАНИЕ ВЕЩЕСТВА |
РЕАГЕНТЫ |
|
А) оксид кальция |
1) H2SO4, H2O |
|
Б) азотная кислота |
2) BaSO4, NaOH |
|
В) сульфат железа (II) |
3) Au, Fe2O3 |
|
4) Zn, NaOH |
Ответ: ![]()
Часть 2
Для заданий 20-22 дайте развернутый ответ.
20. Используя метод электронного баланса, расставьте коэффициенты в уравнении реакции, схема которой CuS + O2 → SO2 + CuO. Определите окислитель и восстановитель.
21. Какую массу гидроксида калия следует добавить к 200 г 9,8%-ного раствора серной кислоты для полной нейтрализации этого раствора?
22. Даны вещества FeSO4, Fe, FeO, разбавленная HNO3, Na. Используя воду и необходимые вещества только из этого списка, получите в две стадии гидроксид железа (II). Для реакции ионного обмена напишите сокращенное ионное уравнение.