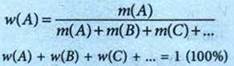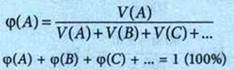Химия - учебно-практический справочник
Решение задач по химическим формулам и на нахождение формулы вещества - Вычисления в химии
Мz — молекулярная масса вещества;
М — молярная масса вещества;
Mr(NaCl) =23 + 35,5 = 58,5;
M(NaCl) = 58,5 г/моль;
v — количество вещества.
v = m/M, где m — масса вещества, М — молярная масса вещества.
Задача
Вычислите количество вещества углекислого газа, которое соответствует его массе 22 г.

v = N/ Na, Na — число Авогадро, N — число молекул (атомов, ионов и т. д.)
Na = 6,02 ∙ 1023 моль-1.
Задача
Вычислите число атомов металла натрия количеством вещества 2 моль.

Задача
Вычислите число молекул, содержащихся в углекислом газе количеством вещества 2 моль.
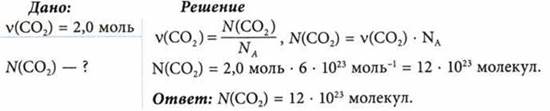
Задача
Вычислите массу углекислого газа, которая соответствует количеству вещества 0,25 моль.

Объем газа количеством вещества 1 моль при нормальных условиях называют молярным и обозначают Vm (22 л/моль).
V = V/Vm, V — объем газа
V = v ∙ Vm
Объем одного киломоля называют киломолярным и измеряют в м3/кмоль (Vm = 22,4 м3/кмоль).
Задача
Найдите объем углекислого газа количеством вещества 2 моль.
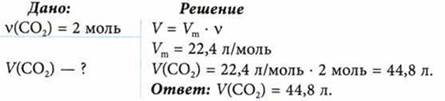
Задача
Вычислите объем, который занимает кислород массой 96 г, при нормальных условиях.

Относительная плотность первого газа по второму — отношение массы определенного газа к массе такого же объема другого газа при одинаковых условиях (т. е. при соответствующих температуре и давлении).
D — относительная плотность газа.
![]() m1 и m2 — массы первого и второго газов.
m1 и m2 — массы первого и второго газов.
![]() М1 и М2 — молярные массы первого и второго газов.
М1 и М2 — молярные массы первого и второго газов.
![]() 2 — относительная молекулярная масса водорода.
2 — относительная молекулярная масса водорода.
![]() 32 — относительная молекулярная масса кислорода.
32 — относительная молекулярная масса кислорода.
![]() 29 — относительная молекулярная масса воздуха.
29 — относительная молекулярная масса воздуха.
Молярная масса газа равна его плотности относительно другого газа, умноженной на молярную массу последнего.
М = 2D, М = 32D, М = 29D
М = Vm ∙ ρ, ρ — плотность газа, измеренная в г/л.
Задача
Вычислите плотность и относительную плотность углекислого газа по водороду.

Задача
Определите молярную массу кислорода, если масса 1 л его при н. у. равна 1,43 г/л.

Задача
Определите массовые доли элементов в оксиде меди(I).

Задача
Какой объем воздуха потребуется, чтобы сжечь 50 м3 газа, содержащего 90% метана, 5% этана, 3% оксида углерода(IV), 2% азота?
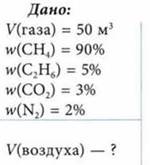
Решение
Из всех составляющих газа горят метан и этан. Найдем объемы метана и этана в смеси газов:

При неизменном давлении объемы газов, которые реагируют и образуются, относятся между собой как небольшие целые числа, и коэффициенты в уравнении реакции показывают число объемов реагирующих и образующихся газов. Найдем объем кислорода, который необходим для сжигания метана и этана:
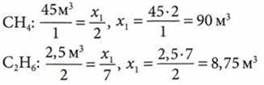
Общий объем кислорода: 90 м3 + 8,75 м3 = 98,75 м3.
В воздухе содержится 21% кислорода. Найдем объем необходимого для реакции воздуха:

Ответ: V(воздуха) = 470 м3.
Количественный состав смесей
Основные расчетные формулы
|
Понятие |
Формула |
Единица измерения |
|
Массовая доля компонента А в смеси веществ А, В, С |
|
Доли единицы, проценты |
|
Объемная доля компонента А в смеси веществ А, В, С |
|
Доли единицы, проценты |
Задача
Рассчитайте массу меди в бронзе массой 500 г (сплав 90% Сu и 10% Sn).

Задача
Определите состав (в объемных%) смеси оксида углерода(II) и оксида углерода(IV), если при пропускании 5 л смеси газов (н. у.) через раствор гидроксида натрия масса последнего увеличилась на 5,9 г.
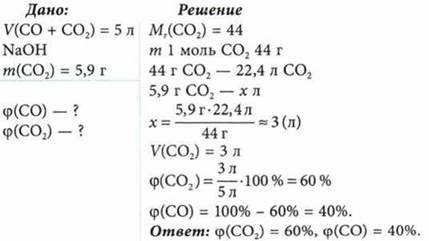
Задача
Составьте химическую формулу оксида, если известно, что 2,3 массовые части натрия сочетаются с 0,8 массовой части кислорода.
Решение
Чтобы найти стехиометрическое соотношение числа атомов в соединении, поделим массовые части элементов на относительные атомные массы: Ar(Na) = 23; Аг(O) = 16.
![]()
Для получения целых соотношений умножим их на 20:
n(Na) : n(О) = (0,1 ∙ 20) : (0,05 ∙ 20) = 2 : 1.
На 2 атома натрия приходится 1 атом кислорода. Следовательно, формула соединения — Na2O.
Ответ: оксид Na2O.
Задача
Известно соединение, содержащее 27,928% фосфора и 72,072% серы. Найдите его простейшую формулу.