Химия ЕГЭ - 1000 заданий с ответами и решениями - 2018 год
Ионный (правило В.В. Марковникова) и радикальный механизмы реакций в органической химии - Химическая реакция - ТЕОРЕТИЧЕСКИЕ ОСНОВЫ ХИМИИ
Тесты с кратким ответом с решениями
1. Радикалами являются частицы:
1) СН3
2) F2
3) С8Н18
4) ОН
5) Аr
6) Сl
2. По радикальному механизму протекает
1) хлорирование метана
2) хлорирование этилена
3) хлорирование пропена при 500°С
4) горение пропана
5) гидратация пропена
6) взаимодействие этилена с бромоводородом
3. По ионному механизму протекают реакции, уравнения которых
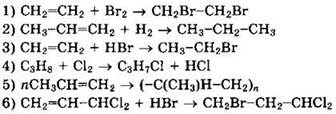
4. В соответствии с правилом В.В. Марковникова происходит взаимодействие
1) бутена-2 с бромоводородом
2) водорода с пропеном
3) бутена-1 с водой
4) хлороводорода с пентеном-1
5) З-фторпропена-1 с бромоводородом
6) воды с пропеном
5. В соответствии с правилом Зайцева происходит
1) дегидратация бутанола-1
2) дегидрогалогенирование 2-хлорпропана
3) дегидрогалогенирование 2-хлорбутана
4) дегидратация бутанола-2
5) дегидратация пентанола-2
6) дегидрогалогенирование 1-хлорбутана
Тесты с кратким ответом для самостоятельного решения
6. Радикалами являются частицы
![]()
7. По радикальному механизму протекает
1) хлорирование толуола в присутствии АlСl3
2) бромирование пропена
3) хлорирование толуола при УФ-облучении
4) полимеризация этилена
5) гидратация этилена
6) взаимодействие бромэтана с натрием
8. По ионному механизму протекают реакции, уравнения которых
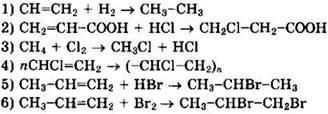
9. В соответствии с правилом В.В. Марковникова происходит взаимодействие
1) гидратация бутена-1
2) гидрогалогенирование пропена
3) гидратация бутена-2
4) гидрогалогенирование бутена-1
5) дегидратация бутанола-2
6) гидрирование бутена-1
10. Реакция замещения протекает между веществами
1) бутаном и 10%-ной азотной кислотой
2) бутеном-2 и раствором брома
3) 2-метилпропаном и бромом
4) бензолом и хлором в присутствии АlСl3
5) этеном и раствором перманганата калия
6) 2-хлорпропаном и спиртовым раствором щелочи
Ответы на тесты раздела 1.4.10
1. 146 2. 134 3. 136 4. 346 5. 345 6. 345 7. 346 8. 256 9. 124 10. 134
Решения тестов раздела 1.4.10
Решение 1. Радикалы — это частицы, имеющие неспаренные электроны. Радикалы образуются при гомолитическом разрыве ковалентной связи. Так, при разрыве связи С-Н в метане образуются два радикала — метил и атом водорода: ![]() При разрыве связи в молекуле воды образуются два радикала — гидроксил и атом водорода:
При разрыве связи в молекуле воды образуются два радикала — гидроксил и атом водорода: ![]() При разрыве связи Сl—Сl образуются два радикала — два атома хлора:
При разрыве связи Сl—Сl образуются два радикала — два атома хлора: ![]() Таким образом, среди перечисленных соединений радикалами являются: метил СН3 — ответ 1, гидроксил ОН — ответ 4, хлор Сl — ответ 6. Молекулы F2, C8H18 и атом Аr неспаренных электронов не имеют и радикалами не являются.
Таким образом, среди перечисленных соединений радикалами являются: метил СН3 — ответ 1, гидроксил ОН — ответ 4, хлор Сl — ответ 6. Молекулы F2, C8H18 и атом Аr неспаренных электронов не имеют и радикалами не являются.
Ответ: 146.
Решение 2. Хлорирование алканов, и в частности метана, — это реакция замещения, которая идет на свету или при нагревании по радикальному механизму: ![]()
![]() — ответ 1. Хлорирование алкенов, и в частности этилена, — это реакция присоединения, которая идет по электрофильному механизму:
— ответ 1. Хлорирование алкенов, и в частности этилена, — это реакция присоединения, которая идет по электрофильному механизму: ![]() Взаимодействие хлора с пропеном при 500° С — это реакция замещения, которая идет по радикальному механизму:
Взаимодействие хлора с пропеном при 500° С — это реакция замещения, которая идет по радикальному механизму: ![]() — ответ 3. При обычных условиях — это реакция присоединения, которая идет по электрофильному механизму:
— ответ 3. При обычных условиях — это реакция присоединения, которая идет по электрофильному механизму: ![]()
![]() Горение алканов, и в частности пропана, идет по радикальному механизму:
Горение алканов, и в частности пропана, идет по радикальному механизму: ![]()
![]() — ответ 4. Гидратация пропена — это электрофильная реакция присоединения:
— ответ 4. Гидратация пропена — это электрофильная реакция присоединения: ![]()
![]() Взаимодействие этилена с бромоводородом — это электрофильная реакция присоединения:
Взаимодействие этилена с бромоводородом — это электрофильная реакция присоединения: ![]()
Ответ: 134.
Решение 3. Реакции присоединения к алкенам галогенов (реакция 1), галогеноводородов (реакции 3 и 6), воды, как правило, идут по электрофильному, то есть ионному, механизму. Реакции присоединения к алкенам водорода (реакция 2) и полимеризации алкенов (реакция 5) идут при нагревании в присутствии катализатора по радикальному механизму. Реакция хлорирования алканов (реакция 4) идет на свету или при нагревании по радикальному механизму.
Ответ: 136.
Решение 4. Правило Марковникова: при присоединении галогеноводородов или воды к алкенам водород преимущественно присоединяется к более гидрогенизированному атому углерода при двойной связи.
В бутене-2 СН3-СН=СН-СН3 атомы углерода при двойной связи равноценны, водород в равной степени присоединяется к каждому из них. Очевидно, что к реакциям гидрирования алкенов правило Марковникова не применимо. Реакции бутена-1 с водой (реакция 3), хлороводорода с пентеном-1 (реакция 4) и воды с пропеном (реакция 6) идут по правилу Марковникова:
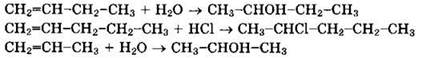
Взаимодействие З-фторпропена-1 с бромоводородом идет вопреки правилу Марковникова:
![]()
Подобное протекание реакции имеет место, если к менее гидрогенизированному атому углерода при двойной связи присоединена не электроно-донорная группа -СН3, -С2Н5 или др., как в углеводородах, к которым, собственно говоря, и применимо правило Марковникова, а электроноакцепторная группа -CH2F, -СНСl2, -СНО, -СООН и др.
Ответ: 346.
Решение 5. Правило Зайцева: при дегидрогалогенировании галогенопроизводных и дегидратации спиртов водород уходит от менее гидрогенизированного атома углерода.
Дегидратация бутанола-1 (реакция 1) идет не по правилу Зайцева — водород может уходить только из положения 2:
![]()
Дегидрогалогенирование 2-хлорпропана (реакция 2) идет не по правилу Зайцева, поскольку атомы углерода в положениях 1 и 3 равноценны:
![]()
Дегидрогалогенирование 2-хлорбутана (реакция 3) идет по правилу Зайцева с образованием бутена-2: ![]()
![]()
Дегидратация бутанола-2 (реакция 4) и пентанола-2 (реакция 5) идет по правилу Зайцева с образованием бутена-2 и пентена-2 соответственно:
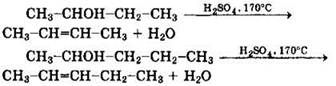
Дегидрогалогенирование 1-хлорбутана (реакция 6) идет не по правилу Зайцева — водород может уходить только из положения 2:
![]()
Ответ: 345.