Химия ОГЭ - Основной государственный экзамен - Комплекс материалов для подготовки учащихся - Д.Ю. Добротин - 2018 год
Периодический закон Д.И. Менделеева. Закономерности изменения свойств элементов и их соединений в связи с положением в периодической системе химических элементов - Вещество - ПРИМЕРЫ РЕШЕНИЙ ЗАДАНИЙ И ЗАДАНИЯ ДЛЯ САМОСТОЯТЕЛЬНОЙ РАБОТЫ ПО СОДЕРЖАТЕЛЬНЫМ БЛОКАМ
Примеры решения заданий
Пример 1.
В ряду химических элементов Si → Р → S
1) уменьшается число протонов в ядре
2) уменьшается электроотрицательность
3) увеличивается число электронов во внешнем электронном слое
4) увеличивается радиус атомов
5) усиливаются неметаллические свойства
Ответ: ![]()
Для начала воспользуемся Периодической системой химических элементов Д.И. Менделеева и найдем в ней предложенный ряд химических элементов Si → Р → S. Как видно эти элементы расположены в IV, V и VI группах III-го периода. Элементы расположены в порядке возрастания зарядов ядер атомов. Опираясь на знание закономерностей изменений свойств атомов, сразу можно исключить неправильный ответ 1, т.к. с ростом зарядов ядер закономерно возрастает и число протонов. Вариант ответа 4 также неверен, т.к. с ростом зарядов ядер увеличивается и число электронов во внешнем слое. Внимание, у нас есть такой ответ под номером 3. Значит, один правильный ответ мы уже определили.
Остались для рассмотрения ответы 2 и 5. Они тоже взаимосвязаны. Электроотрицательность возрастает с ростом числа электронов во внешнем слое (электроотрицательность - способность удерживать “свои” и притягивать “чужие” электроны), а чем больше электронов во внешнем слое, тем сильнее проявляются неметаллические свойства. Отсюда, ответ 2 - неверен, а вот ответ 5 - правильный.
Запись ответа будет выглядеть так: 35.
Пример 2.
Сходство натрия, магния и алюминия проявляется в том, что
1) в их атомах одинаковое число протонов
2) во внешнем электронном слое их атомов находится одинаковое число электронов
3) простые вещества проявляют металлические свойства
4) в соединениях проявляют только положительные степени окисления
5) соответствующие им высшие оксиды являются основными
Ответ: ![]()
Для выполнения задания необходимо дать сравнительную характеристику двух элементов и соответствующих им простых веществ. Для этого необходимо воспользоваться Периодической системой химических элементов.
Натрий, магний и алюминий - химические элементы, имеющие порядковые номера 11, 12, 13 (соответственно), расположенные в третьем периоде, но в разных группах Периодической системы.
Следовательно, у этих элементов разное число протонов, т.к. оно равно порядковому номеру; одинаковое число электронных слоёв, т.к. расположены в одном периоде; разное число электронов во внешнем электронном слое.
Этим элементам соответствуют простые вещества металлы, а следовательно, они могут только отдавать электроны и в соединениях проявлять только положительные степени окисления.
Для формулирования правильного вывода о свойствах оксидов следует напомнить, что у элементов, расположенных в одном периоде, основные свойства оксидов слева направо ослабевают и усиливаются кислотные свойства. Алюминий - элемент, образующий амфотерный оксид.
Таким образом, сходство элементов верно сформулировано в вариантах ответа 3 и 4. Ответ: 34.
Задания для самостоятельной работы
81. Общим для натрия и алюминия является
1) наличие 12 протонов в ядрах их атомов
2) нахождение валентных электронов в третьем электронном слое
3) образование простых веществ-металлов
4) существование в природе в виде двухатомных молекул
5) образование ими высших оксидов с общей формулой Э2О
Ответ: ![]()
82. Общим для магния и кальция является
1) наличие 20 электронов в атомах
2) нахождение валентных электронов в третьем электронном слое
3) наличие двух электронов во внешнем электронном слое
4) существование атомов в виде простых веществ-неметаллов
5) способность образовывать основные оксиды
Ответ: ![]()
83. В ряду химических элементов: Аl → Si → Р - происходит увеличение (усиление)
1) числа протонов в ядрах атомов
2) числа заполняемых электронных слоёв в атомах
3) радиуса атомов
4) металлических свойств
5) степени окисления в высших оксидах
Ответ: ![]()
84. В ряду химических элементов: Si → Аl → Mg - происходит уменьшение (ослабление)
1) заряда ядер атомов
2) числа валентных электронов в атомах
3) радиуса атомов
4) металлических свойств
5) основных свойств высших оксидов
Ответ: ![]()
85. В ряду химических элементов: Se → S → О - происходит увеличение (усиление)
1) заряда ядер атомов
2) числа электронных слоёв в атомах
3) радиуса атомов
4) электроотрицательности
5) неметаллических свойств
Ответ: ![]()
86. В ряду химических элементов Ge → Si → С
1) уменьшается радиус атомов
2) возрастает способность атомов отдавать электроны
3) увеличиваются заряды ядер атомов
4) уменьшается относительная атомная масса
5) увеличивается степень окисления в высших оксидах
Ответ: ![]()
87. В ряду химических элементов Аl → Mg → Na
1) уменьшается радиус атомов
2) усиливаются металлические свойства
3) уменьшаются заряды ядер атомов
4) увеличивается число электронов во внешнем электронном слое атомов
5) увеличивается число электронных слоёв в атомах
Ответ: ![]()
88. В ряду химических элементов Li → Be → В
1) увеличивается электроотрицательность
2) уменьшаются металлические свойства
3) уменьшаются заряды ядер атомов
4) уменьшается число электронов во внешнем электронном слое атомов
5) увеличивается число заполненных электронных слоёв в атомах
Ответ: ![]()
89. В ряду химических элементов I → Вr → Сl
1) увеличивается степень окисления элементов в высших оксидах
2) уменьшается число валентных электронов в атомах
3) усиливаются неметаллические свойства
4) увеличиваются заряды ядер атомов
5) уменьшаются радиусы атомов
Ответ: ![]()
90. В каких рядах элементы расположены в порядке усиления их окислительных свойств?
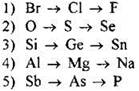
Ответ: ![]()
91. В ряду химических элементов Be → В → С
1) увеличивается число электронов во внешнем электронном слое атомов
2) усиливаются металлические свойства
3) уменьшается радиус атомов
4) увеличивается число электронных слоёв в атомах
5) уменьшаются заряды ядер атомов
Ответ: ![]()
92. В ряду химических элементов F → О → N
1) уменьшается число электронов во внешнем электронном слое атомов
2) усиливаются неметаллические свойства
3) уменьшается радиус атомов
4) увеличивается число электронных слоёв в атомах
5) уменьшаются заряды ядер атомов
Ответ: ![]()
93. В ряду химических элементов Аl → Р → Сl
1) увеличивается электроотрицательность
2) уменьшаются заряды ядер атомов
3) возрастают металлические свойства
4) уменьшаются радиусы атомов
5) уменьшается число электронов во внешнем электронном слое атомов
Ответ: ![]()
94. В ряду химических элементов Si → Аl → Mg
1) уменьшается электроотрицательность
2) увеличиваются заряды ядер атомов
3) ослабевают неметаллические свойства
4) уменьшаются радиусы атомов
5) увеличивается число заполненных электронных слоёв атомов
Ответ: ![]()
95. В ряду химических элементов N → О → F
1) усиливаются неметаллические свойства
2) уменьшается электроотрицательность
3) уменьшается число электронов во внешнем электронном слое
4) увеличивается число заполненных электронных слоёв
5) уменьшается радиус атомов
Ответ: ![]()
96. В порядке уменьшения числа электронов во внешнем слое расположены химические элементы следующих рядов:
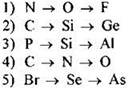
Ответ: ![]()