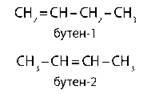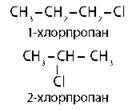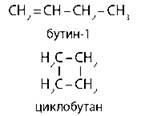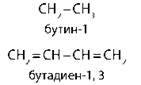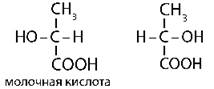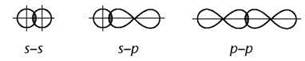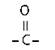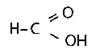Химия - Универсальный справочник школьника подготовка к ЕГЭ
ЭКСПРЕСС-ПОМОЩНИК - Урок 4 - ОРГАНИЧЕСКАЯ ХИМИЯ
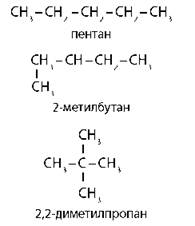
Структурная изомерия
|
Виды |
Примеры |
|
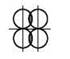
Изомерия углеродного скелета |
|
|
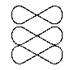
Изомерия положения кратных связей |
|
|
Изомерия положения заместителей |
|
|
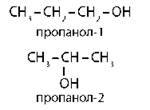
Изомерия положения функциональных групп |
|
Изомерия между классами соединений (межклассовая)
|
Виды |
Примеры |
|
алкены ⇔ циклоалканы |
|
|
алкины ⇔ алкадиены |
|
|
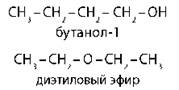
одноатомные спирты ⇔ простые эфиры |
|
|
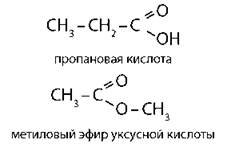
карбоновые кислоты ⇔ сложные эфиры |
|
Изомерия между классами соединений (межклассовая)
|
Конфигурационная изомерия |
|
|
Оптическая изомерия |
|
|
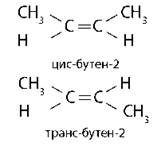
Геометрическая изомерия |
|
|
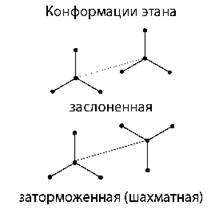
Конформационная изомерия |
|
Связи в молекулах органических веществ
|
Типы связей |
Примеры |
|
по кратности связи |
|
|
одинарные |
длина связи 0,154 нм |
|
двойные |
длина связи 0,134 нм |
|
тройные |
-С≡С– длина связи 0,120 нм |
|
ароматические |
длина связи 0,140 нм |
|
По способу перекрывания электронных облаков |
|
|
σ-связи |
электронные облака перекрываются на линии, которая соединяет центры атомов |
|
π-связи |
место перекрывания электронных облаков не лежит на линии, которая соединяет центры атомов |
Гибридизация
|
Тип |
s |
р |
Гибридные орбитали |
Форма |
Пример |
|
sp |
Одна s-орбиталь |
Одна р-орбиталь |
Две sp-орбитали |
Линейная |
C2Н2 |
|
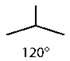
sp2 |
Одна s-орбиталь |
Две р-орбитали |
Три sp2-орбитали |
Плоская тригональная |
C2Н4 |
|
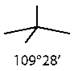
sp3 |
Одна s-орбиталь |
Три р-орбитали |
Четыре sp3-орбитали |
Тетраэдрическая |
CН4 |
Функциональная группа. Радикал
|
Функциональная группа |
Постоянная группа атомов, которая определяет характерные свойства вещества: -OH, -COOH и т. д. |
|
Радикал |
Остаток молекулы углеводорода, который образуется вследствие удаления одного или нескольких атомов водорода -СH3 метил -С2H5 этил -С3H7 пропил |
Классификация по качественному составу функциональных групп
|
Класс органических соединений |
Функциональная группа |
Общая формула |
Состав соединения |
|
Галогенопроизводные углеводородов |
-F, -Cl -Br, -I (-Hal) |
R-Hal |
CnH2n+1Hal |
|
Одноатомные спирты |
-OH |
R-OH |
CnH2n+2O |
|
Фенолы |
-OH |
Ar-OH |
CnH2n-6O |
|
Простые эфиры |
-O-R |
R-O-R’ |
CnH2n+2O |
|
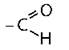
Альдегиды |
|
|
CnH2nO |
|
Кетоны |
|
|
CnH2nO |
|
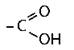
Карбоновые кислоты |
|
|
CnH2nO2 |
|
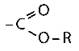
Сложные эфиры |
|
|
CnH2nO2 |
|
Нитросоединения |
-NO2 |
R-NO2 |
CnH2n+1NO2 |
|
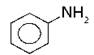
Амины (первичные) |
-NH2 |
R-NH2 |
CnH2n+3N |
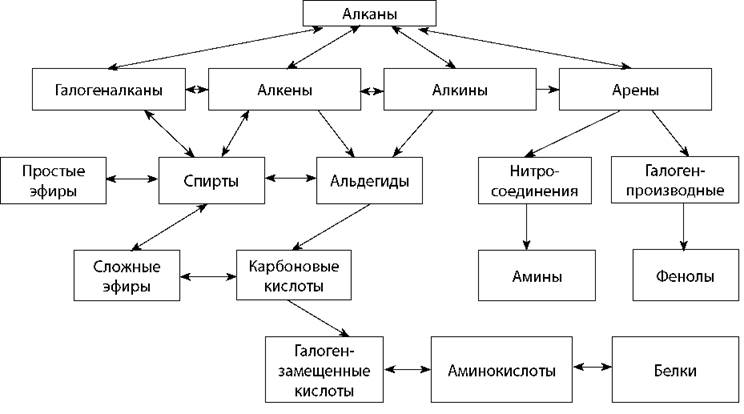
Взаимосвязь различных классов органических веществ
Качественные реакции на органические вещества
|
Вещество |
Реактив, условие |
Признаки реакции |
|
CH2 = CH2 |
1. Раствор KMnO4, Н+ |
1. Обесцвечивание раствора |
|
2. Раствор Br2 (бромная вода) |
2. Обесцвечивание раствора |
|
|
C2H5OH |
CuO |
Изменение цвета проволоки, выделение паров с фруктовым запахом |
|
|
Сu(OН)2 |
Образование ярко-синего раствора |
|
|
1. Раствор Br2 (бромная вода) |
1. Выпадение белого осадка |
|
2. Раствор FeCl3 |
2. Фиолетовое окрашивание |
|
|
|
1. Cu(OH)2, t |
1. Образование красного (морковного) осадка Cu2O |
|
2. Ag2O (аммиачный раствор), t |
2. Образование «серебряного зеркала» |
|
|
СН3СOOН |
1. Лакмус |
1. Красное окрашивание |
|
2. Раствор Na2CO3 |
2. Выделение газа, CO2 |
|
|
НСOOН |
1. Лакмус |
1. Красное окрашивание |
|
|
2. Раствор KMnO4, Н+ |
2. Обесцвечивание раствора |
|
|
3. Раствор Na2CO3 |
3. Выделение газа, CO2 |
|
|
4. Ag2O, аммиачный раствор |
4. Образование «серебряного зеркала», выделение CO2 |
|
C17H33COOH |
1. Раствор Вr2 (бромная вода) |
1. Обесцвечивание раствора |
|
2. Раствор KMnO4 |
2. Обесцвечивание раствора |
|
|
C17H35COONa раствор мыла |
1. H+ |
1. Образование белых хлопьев |
|
C6H12O6 |
2. Cu(OH)2 |
2. Ярко-синее окрашивание; при нагревании образование красного (морковного) осадка |
|
3. Ag2O (аммиачный раствор), t |
3. Образование «серебряного зеркала» |
|
|
(C6H10O5)n крахмал |
Раствор I2 |
Синее окрашивание |
|
|
Раствор Вr2 (бромная вода) |
Выпадение белого осадка |
|
Белок яичный (раствор) |
1. HNO3 |
1. Образование осадка желтого цвета |
|
2. Cu(OH)2 |
2. Фиолетовое окрашивание |