Химия - Универсальный справочник школьника подготовка к ЕГЭ
Аминокислоты - Аминокислоты как амфотерные органические соединения. Белки - ОРГАНИЧЕСКАЯ ХИМИЯ
Строение аминокислот
Аминокислоты — гетерофункциональные соединения, которые обязательно содержат две функциональные группы: аминогруппу —NH2 и карбоксильную группу —СООН, связанные с углеводородным радикалом.
Общую формулу простейших аминокислот можно записать так:
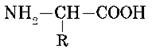
Так как аминокислоты содержат две различные функциональные группы, которые оказывают влияние друг на друга, характерные реакции отличаются от характерных реакций карбоновых кислот и аминов.
Свойства аминокислот
Аминогруппа —NH2 определяет основные свойства аминокислот, т. к. способна присоединять к себе катион водорода по донорно-акцепторному механизму за счет наличия свободной электронной пары у атома азота.
Группа —СООН (карбоксильная группа) определяет кислотные свойства этих соединений. Следовательно, аминокислоты — это амфотерные органические соединения.
Со щелочами они реагируют как кислоты:
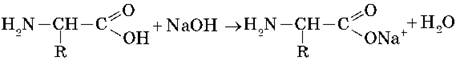
С сильными кислотами — как основания-амины:
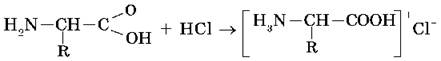
Кроме того, аминогруппа в аминокислоте вступает во взаимодействие с входящей в ее состав карбоксильной группой, образуя внутреннюю соль:
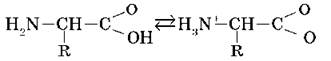
Ионизация молекул аминокислот зависит от кислотного или щелочного характера среды:
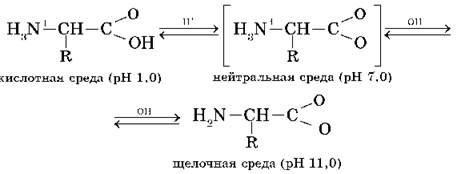
Так как аминокислоты в водных растворах ведут себя как типичные амфотерные соединения, то в живых организмах они играют роль буферных веществ, поддерживающих определенную концентрацию ионов водорода.
Аминокислоты представляют собой бесцветные кристаллические вещества, плавящиеся с разложением при температуре выше 200 °С. Они растворимы в воде и нерастворимы в эфире. В зависимости от радикала R— они могут быть сладкими, горькими или безвкусными.
Аминокислоты подразделяют на природные (обнаруженные в живых организмах) и синтетические. Среди природных аминокислот (около 150) выделяют протеиногенные аминокислоты (около 20), которые входят в состав белков. Они представляют собой L-формы. Примерно половина из этих аминокислот относятся к незаменимым, т. к. они не синтезируются в организме человека. Незаменимыми являются такие кислоты, как валин, лейцин, изолейцин, фенилаланин, лизин, треонин, цистеин, метионин, гистидин, триптофан. В организм человека данные вещества поступают с пищей. Если их количество в пище будет недостаточным, нормальное развитие и функционирование организма человека нарушаются. При отдельных заболеваниях организм не в состоянии синтезировать и некоторые другие аминокислоты. Так, при фенилкетонурии не синтезируется тирозин.
- ЗАПОМНИ. Аминокислоты реагируют друг с другом и образуют высокомолекулярные соединения; группа атомов ![]() называется пептидной или амидной группой.
называется пептидной или амидной группой.
Важнейшим свойством аминокислот является способность вступать в молекулярную конденсацию с выделением воды и образованием амидной группировки —NH—CO—, например:
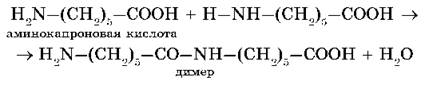
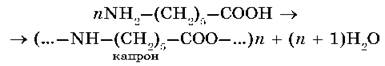
Получаемые в результате такой реакции высокомолекулярные соединения содержат большое число амидных фрагментов и поэтому получили название полиамидов.
К ним, кроме названного выше синтетического волокна капрона, относят, например, и энант, образующийся при поликонденсации аминоэнантовой кислоты. Для получения синтетических волокон пригодны аминокислоты с расположением амино- и карбоксильной групп на концах молекул.
Полиамиды α-аминокислот называются пептидами. В зависимости от числа остатков аминокислот различают дипептиды, трипептиды, полипептиды. В таких соединениях группы —NH—CO— называют пептидными.
- ЗАПОМНИ. Аминогруппа — NH2 определяет основный характер аминокислот. Карбоксильная группа (СООН) определяет кислотные свойства аминокислот. Аминокислоты в водных растворах ведут себя как амфотерные соединения.
Изомерия и номенклатура
Изомерия аминокислот определяется различным строением углеродной цепи и положением аминогруппы, например:
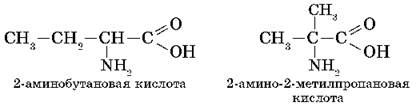
Широко распространены также названия аминокислот, в которых положение аминогруппы обозначается буквами греческого алфавита: α, β, γ и т. д. Так, 2-аминобутановую кислоту можно назвать также α-аминокислотой:
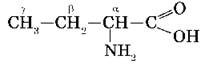
В биосинтезе белка в живых организмах участвуют 20 аминокислот.