Настольная книга учителя химии 10 класс - поурочные разработки
СТРОЕНИЕ КАРБОКСИЛЬНОЙ ГРУППЫ. АЛЬДЕГИДЫ И КЕТОНЫ: НОМЕНКЛАТУРА, ИЗОМЕРИЯ И ФИЗИЧЕСКИЕ СВОЙСТВА - КИСЛОРОДОСОДЕРЖАЩИЕ СОЕДИНЕНИЯ
Цели урока. Рассмотреть гомологические ряды, виды изомерии и номенклатуру альдегидов и кетонов. Разобрать строение карбоксильной группы и на этой основе подчеркнуть особенное для альдегидов в сравнении с кетонами. Познакомить учащихся с физическими свойствами представителей этих классов соединений и их значением в живой природе и повседневной жизни человека.
Оборудование: демонстрационные образцы: глюкоза, ванилин, формалин, ацетон, любое чистящее или моющее средство (порошок или жидкость) с лимонной отдушкой; модели молекул Стюарта — Бриглеба, плакат с формулами ванилина, цитраля, феромонов (для профильных классов).
I. Как уксусный альдегид двух химиков поссорил
Для занимательного построения начала урока учитель делает следующее сообщение. В конце XVIII в. химики интенсивно изучали свойства известных органических соединений. В 1782 г. К. Шееле, окисляя этиловый спирт оксидом марганца (IV) в серной кислоте, заметил, что помимо основного продукта — уксусной кислоты — образовывалось еще какое-то резко пахнущее соединение, выделить которое не удалось. В последующие годы новый «кислородный эфир» упоминался в работах Дабъ, А. Фуркруа, Л. Воклена. В 1821 г. Иоганн Вольфганг Дёберейнер окислял этиловый спирт в присутствии платинового катализатора и выделил некоторое количество смеси исходного спирта с продуктами его окисления. Многие химики, в том числе и Ю. Либих, сомневались, что в этой смеси содержится неизвестное вещество. Дёберейнер отправил полученный им образец Либиху, из которого тот в 1835 г. выделил чистое вещество, содержащее на два атома водорода меньше, чем этанол. Ученый установил его состав (С2Н4О) объявил, что получил новое вещество, которому дал название Alkohol dehydrogenatus — безводородный алкоголь или сокращенно альдегид. В ответ на претензии Дёберейнера на приоритет открытия Либих в характерной ему едкой манере заметил, что тот имеет столько же оснований претендовать на открытие альдегида, сколько ньютоновское яблоко — на открытие закона всемирного тяготения.
Поскольку первый из известных альдегидов содержал два атома углерода, начались попытки получения первого представителя гомологического ряда. Они были неудачными вплоть до 1868 г., когда немецкий химик-органик Август Вильгельм Гофман, пропуская пары метилового спирта над раскаленной платиновой спиралью, получил газообразное вещество состава СН2О. Это был формальдегид — родоначальник ряда альдегидов, общая формула которых
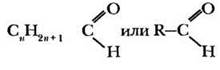
II. Электронное и пространственное строение карбонильной группы
После краткого исторического вступления учитель предлагает ребятам вопрос: если известно, что альдегиды содержат на два атома водорода меньше, чем предельные спирты, как это отражается на их строении?
Хорошо, если учащиеся предлагают вариант: в молекуле должна быть двойная связь (кто-то из профильного класса может предположить наличие цикла). А как же быть с альдегидом, содержащим один атом углерода — СН2О? Без нарушения валентностей атомов цикл построить нельзя, остается единственный вариант: атомы углерода и кислорода связаны двойной связью.
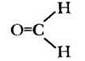
Так легко справиться с разгадкой строения альдегидов не удавалось до середины XIX в. Получается, что современный школьник, вооруженный знанием теории химического строения А. М. Бутлерова,— более грамотный химик, чем знаменитые ученые рубежа XVIII—XIX вв.!
После того как учитель дал определения понятий альдегид и кетон, необходимо остановиться на электронном и пространственном строении карбонильной группы.
Учащиеся могут утверждать, что наличие двойной связи у атома углерода в карбонильной группе предполагает, что этот атом находится в состоянии sp2-гибридизации и поэтому образует три прочные ковалентные σ-связи с тремя соседними атомами: кислорода, углерода или водорода (в альдегиде, углерода — в кетоне). За счет перекрывания негибридизованной p-орбитали атома углерода и p-орбитали кислорода между этими атомами образуется еще одна связь, относящая к π-типу (рис. 25). Электронная плотность π-связи С=O, как наиболее подвижной, смещена от атома углерода к более электроотрицательному атому кислорода. В результате на углероде образуется частичный положительный заряд. Где величина этого заряда больше: в альдегидах или кетонах? Поскольку алкильный радикал обладает большим положительным индуктивным эффектом по сравнению с атомом водорода, частичный положительный заряд на углероде в альдегидах превосходит δ+ в молекулах кетонов:
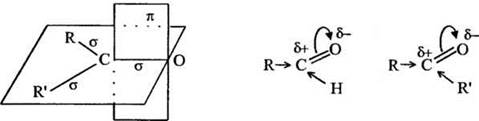
Рис. 25. Электронное строение карбонильной группы
Основной вывод таков: карбонильная группа полярна, атом углерода в ней электрофилен. Это в значительной степени отражается на физических и химических свойствах альдегидов и кетонов.
III. Номенклатура и изомерия альдегидов и кетонов
Как правило, учащимся больше по душе международные названия веществ, поскольку при их составлении есть логика и строгие правила. Поэтому начинать объяснение номенклатуры альдегидов и кетонов следует с требований ИЮПАК. Все изученные правила построения названий остаются в силе, добавляются лишь некоторые особенности.
1. «Отличительными» суффиксами в названиях альдегидов и кетонов служат соответственно -аль и -он.
2. Альдегидная группа может располагаться только на конце молекулы. Нумерация самой длинной цепи в альдегидах начинается с углерода альдегидной группы, а ее положение (цифра 1), как само собой разумеющееся, в названии не указывается. В кетонах же карбонильная группа может находиться и в середине углеродной цепи, поэтому в названии после суффикса -он через дефис указывается ее положение. Нужно помнить, нумеруют самую длинную цепь в кетонах с того конца, к которому ближе карбонильная группа.
3. Если помимо карбонильной группы соединение содержит двойную или тройную связь, то цифру, показывающую ее положение в цепи, удобнее ставить до основы названия (2-бутеналь, 3-пентенон-2).
Как правило, учащиеся легко отвечают на вопрос, какие виды изомерии характерны для альдегидов и кетонов. Если говорить только о соединениях предельного ряда, у альдегидов (помимо межклассовой) есть только изомерия углеродного скелета, а у кетонов добавляется изомерия положения функциональной группы.
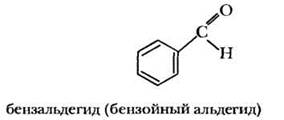
Необходимо сразу же закрепить правила номенклатуры на нескольких примерах. Для учащихся базового уровня — это простейшие структуры соединений предельного ряда и по одному представителю непредельных и ароматических альдегидов: акролеина и бензальдегида.
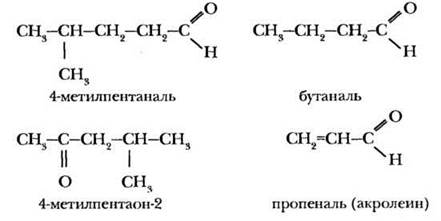
Для учащихся профильных классов задания на отработку номенклатуры можно сделать более интересными. По крайней мере, приведенная ниже информация будет полезна для учителя.
Насекомые общаются между собой, выделяя ничтожные количества органических соединений, имеющих сравнительно небольшие молекулы. Такие вещества называются феромонами. Феромоны делят на половые, возбуждающие, успокаивающие, сбора, тревоги и другие. Чувствительность насекомых к феромонам просто поразительна: самец ночной бабочки большой павлиний глаз, например, чувствует половой феромон самки на расстоянии до 10 км! Синтетические феромоны используются для борьбы с вредными насекомыми путем заманивания их в ловушки, дезориентации в период спаривания, отпугивания.
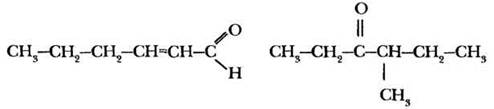
Муравьи для подачи сигнала тревоги выделяют два феромона:
Для закрепления материала этой части урока учитель может предложить учащимся следующие задания.
1. Напишите для альдегида структуры цис- и транс-изомеров и назовите оба вещества (цис-2-гексеналь и транс-2-гексеналь).
2. С помощью какой реакции можно доказать наличие в альдегиде двойной связи? Приведите уравнение (поскольку с раствором перманганата калия может окисляться и альдегидная группа, лучше использовать реакцию с бромной водой).
3. Назовите второй феромон (4-метилгексанон-3).
4. Найдите в молекуле асимметрический атом углерода и изобразите структуры обоих оптических изомеров (С-4).
В заключение этой части урока учитель с помощью ребят выводит общие формулы гомологических рядов предельных альдегидов и кетонов СnН2nО. Выясняется, что они являются межклассовыми изомерами.
IV. Физические свойства альдегидов и кетонов
Характеризуя агрегатное состояние и растворимость в воде низших представителей гомологических рядов альдегидов и кетонов, учитель может упомянуть о том, что карбонильная группа также может участвовать в образовании межмолекулярных водородных связей с молекулами воды, но прочность этих связей значительно меньше, чем для спиртов. Поэтому карбонильные соединения имеют меньшие температуры кипения и плавления, чем спирты с соответствующей молекулярной массой.
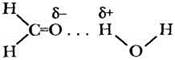
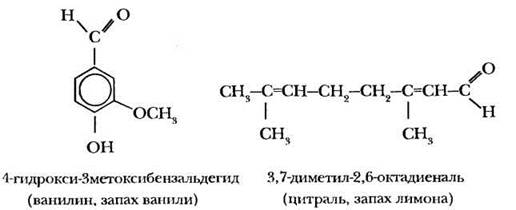
Отличительной чертой многих альдегидов и кетонов является их запах. Для низших представителей гомологических рядов он резкий и часто неприятный. Высшие альдегиды и кетоны, особенно непредельные или ароматические, входят в состав эфирных масел и содержатся во многих цветах, фруктах, плодах, душистых и пряных растениях. Получается, что мы сталкиваемся с альдегидами и кетонами практически ежедневно! Учитель демонстрирует пищевой ванилин и какое-либо средство бытовой химии с лимонной отдушкой. Ванилин — это ароматический альдегид, получаемый синтетически, а запах лимона чистящему средству придает синтетический цитраль, по химической структуре являющийся диеновым альдегидом:
Обоняние в мире животных играет чуть ли не большую роль, чем зрение или слух. Например, муравьи по запаху могут определить не только форму предмета, но и его твердость. Для многих видов запах — это основная сигнальная система. Человек среди земных «нюхачей» занимает одно из последних мест. Мы часто в прямом и переносном смысле употребляем фразу «нюх как у собаки». Она не лишена основания: собака улавливает запахи в концентрации, недоступной не только обонянию человека, но и современным приборам. Она, например, может уловить запах масляной кислоты, если в 1 см3 воздуха содержится всего 9000 молекул этого вещества (ребята могут перевести это число в количество вещества, вспомнив заодно число Авогадро, «забытое» в органической химии).
Задание 1
1-й уровень
Даны молекулярные формулы веществ: C9H6O, СН2О, C3H6O, С4Н8О2, С4Н10О, C4H8O. Выберите формулы предельных карбонильных соединений, напишите структуры всех возможных изомеров и назовите их по международной номенклатуре.
2-й уровень
Сколько изомерных альдегидов и сколько кетонов соответствует формуле С5Н10О? Напишите их структурные формулы, назовите по международной номенклатуре.
Задание 2
1-й уровень
Формальдегид объемом 40 л (н. у.) растворили в 200 мл воды. Определите массовую долю вещества в растворе.
2-й уровень
Ванилин имеет молекулярную формулу С8Н8О3. Это вещество плохо растворимо в воде, максимальная концентрация при комнатной температуре составляет 1%. Рассчитайте количество вещества ванилина, содержащегося в 5 л насыщенного раствора, плотность которого считайте равной 1 г/мл.
Задание 3
1-й уровень
По данным элементного анализа органическое вещество содержит 62,0% углерода и 10,4% водорода. При его горении образуется только углекислый газ и вода. Химический анализ показывает наличие одной карбонильной группы. Напишите структурные формулы возможных изомеров этого вещества и назовите их.
2-й уровень
Анализ органического вещества показал наличие в нем карбонильной группы с молекулярной массой, равной 72 г/моль. При сжигании 0,288 г этого вещества образовалось 0,704 г оксида углерода (IV) и 0,288 г воды. Определите молекулярную формулу вещества, напишите структуры всех возможных изомеров и назовите их.