Химия - учебно-практический справочник
Спирты - Кислородсодержащие органические соединения - Органическая химия
Классификация спиртов
Спирты — гидроксильные производные углеводородов различных типов.
|
В зависимости от количества гидроксильных групп |
В зависимости от характера атома углерода (первичные, вторичные, третичные), с которым соединены гидроксильные группы |
В зависимости от характера углеводородного радикала |
|
Одноатомные СН3—СН2—ОН этанол Двухатомные (гликоли)
этандиол-1,2 (этиленгликоль) Трехатомные (триоли)
пропантриол-1,2,3 (глицерол) |
Первичные CH3—CH2—CH2—OH пропанол-1 Вторичные
пропанол-2 Третичные
2-метилпропанол-2 |
Алифатические: насыщенные CH3—CH2—CH2—OH пропанол-1 ненасыщенные СН2 = СН—СН2—ОН аллиловый спирт Алициклические
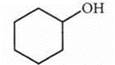
циклогексанол Ароматические
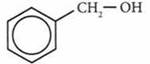
фенилметанол |
Насыщенные одноатомные спирты
Строение. Классификация. Изомерия. Номенклатура
|
Насыщенные одноатомные спирты |
Общая формула СnН2n+1ОН |
|
Валентный угол: |
|
|
Характеристика связей: связи С—О и О—Н сильно полярные |
|
|
Энергия связей: О—Н составляет 456 кДж/моль водородных связей — 20 кДж/моль |
|
|
Номенклатура: название соответствующего алкана + суффикс -ол + цифра положения группы ОН |
|
|
Межмолекулярное взаимодействие благодаря водородной связи
|
|
Виды изомерии |
||
|
структурная |
межклассовая |
|
|
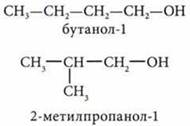
Разветвление углеродного скелета |
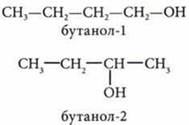
Положение функциональной группы |
Диэтиловый эфир (этоксиэтан) C2H5—O—C2H5 Метилпропиловый эфир (метоксипропан) CH3—O—С3Н7 Это изомеры бутанола |
|
|
|
|
Химические свойства насыщенных одноатомных спиртов
|
Реакции с разрывом связи O—Н |
|
|
с активными металлами (К, Na, Mg, Al)
|
Образуются алкоголяты |
|
с минеральными и органическими кислотами
|
Реакция этерификации (образуются сложные эфиры) |
|
Реакции с участием группы ОН- и атома Н, который расположен возле соседнего атома углерода |
|
|
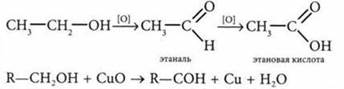
окисление
|
|
|
отщепление водорода
|
дегидрирование, образуются альдегиды |
|
отщепление воды
|
внутримолекулярная дегидратация (t > 160 °С), образуются алкены |
|
отщепление воды и водорода
|
одновременная дегидратация и дегидрогенизация |
|
Реакции с разрывом связи С—O |
|
|
с галогеноводородами
|
образуются галогениды |
|
межмолекулярное отщепление воды
|
межмолекулярная дегидратация (t = 130-140 °С), образуются эфиры |
Получение метанола
1) в процессе сухой перегонки древесины;
2) из синтез-газа:
![]()
Получение этанола
1) гидратацией этена:
![]()
2) спиртовым брожением сахаристых веществ (получают этанол — винный спирт):
![]()
3) при гидролизе клетчатки и последующем брожении продуктов гидролиза:
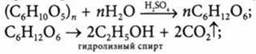
4) восстановлением этаналя:
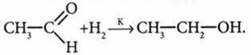
Лабораторный способ получения спиртов
Гидролиз моногалогеналканов под действием водных растворов щелочей:
![]()
Применение спиртов
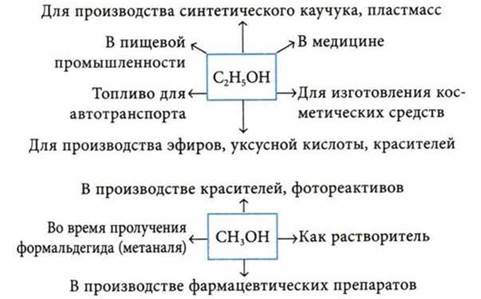
Химические свойства двухатомных спиртов
В реакции могут участвовать как одна, так и две группы —ОН. Вследствие взаимного влияния гидроксильных групп, особенно у α-гликолей (группы —ОН размещены возле соседних углеродных атомов), кислотно-основные свойства гликолей несколько отличны от свойств одноатомных насыщенных спиртов.
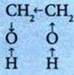 В результате этого воздействия кислотные свойства двухатомных спиртов повышаются: гликоли легко реагируют не только с активными металлами, но и со щелочами и даже гидроксидами тяжелых металлов.
В результате этого воздействия кислотные свойства двухатомных спиртов повышаются: гликоли легко реагируют не только с активными металлами, но и со щелочами и даже гидроксидами тяжелых металлов.
|
этандиол-1,2 (этиленгликоль) |
Взаимодействие с активными металлами |
|
|
|
||
|
Взаимодействие с гидроксидами некоторых тяжелых металлов |
|
|
|
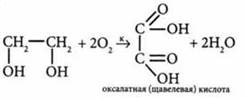
Взаимодействие с галогеноводородами |
|
|
|
Реакция окисления |
|
Химические свойства глицерина
Наблюдается рост кислотных свойств по сравнению с насыщенными одноатомными спиртами.
1) Взаимодействует со щелочными металлами:
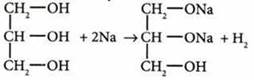
2) взаимодействует с гидроксидами некоторых тяжелых металлов:
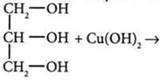 комплексная соль синего цвета
комплексная соль синего цвета
3) взаимодействует с минеральными и органическими кислотами:
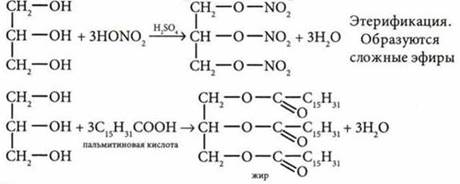
4) Окисление:
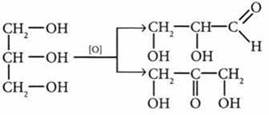 Образуются глицериновый альдегид дигидроксоацетон
Образуются глицериновый альдегид дигидроксоацетон
Получение глицерина
При омылении жиров
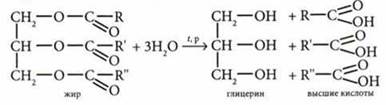
Определение многоатомных спиртов
Взаимодействие с гидроксидом меди(II). Образуется комплексная соль синего цвета.
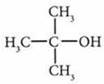
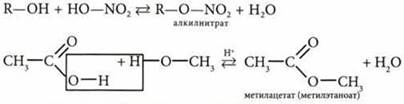
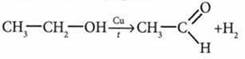
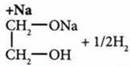 — неполный алкоголят (гликолят)
— неполный алкоголят (гликолят)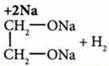 — полный гликолят
— полный гликолят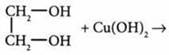 комплексное соединение синего цвета
комплексное соединение синего цвета