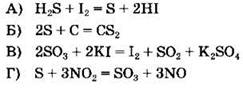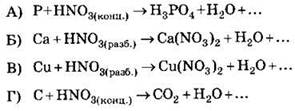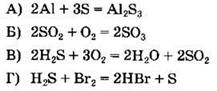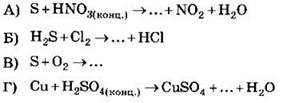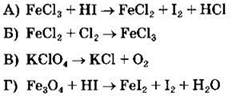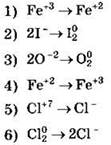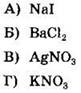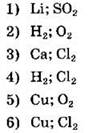Химия самостоятельная подготовка к ЕГЭ - универсальные материалы с методическими рекомендациями, решениями и ответами - 2018 год
Задания для самостоятельной работы - ОСНОВЫ ХИМИИ
1. Электронная конфигурация 1s22s22p63s23p6 соответствует ионам
1) Ti2+
2) Мg2+
3) Fe3+
4) К+
5) S2-
Ответ: ![]()
2. Химические элементы, которые образуют высший оксид с общей формулой R2O5, имеют электронную конфигурацию атомов:
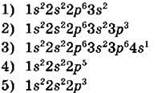
Ответ: ![]()
3. В каких рядах химические элементы расположены в порядке возрастания их атомного радиуса?
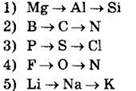
Ответ: ![]()
4. По периоду слева направо уменьшается(-ются)
1) атомный радиус элементов
2) число валентных электронов в атомах
3) электроотрицательность элементов
4) кислотные свойства гидроксидов
5) металлические свойства простых веществ
Ответ: ![]()
5. У элементов подгруппы углерода с увеличением атомного номера уменьшаются
1) атомный радиус
2) заряд ядра атома
3) число валентных электронов в атомах
4) электроотрицательность
5) неметаллические свойства
Ответ: ![]()
6. В ряду химических элементов:
бериллий → бор → углерод
возрастают
1) способность атома отдавать электроны
2) высшая степень окисления
3) низшая степень окисления
4) радиус атома
5) кислотные свойства их высших оксидов
Ответ: ![]()
7. В ряду химических элементов:
Na → Mg → Al → Si
1) увеличивается число валентных электронов в атомах
2) уменьшается число электронных слоев в атомах
3) уменьшается число протонов в ядрах атомов
4) увеличиваются радиусы атомов
5) увеличивается электроотрицательность
Ответ: ![]()
8. В каких рядах простые вещества расположены в порядке усиления металлических свойств?
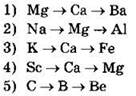
Ответ: ![]()
9. В аммиаке и хлориде бария химическая связь соответственно
1) ионная и ковалентная полярная
2) ковалентная полярная и ионная
3) ковалентная неполярная и металлическая
4) ковалентная неполярная и ионная
Ответ: ![]()
10. Соединениями с ковалентной полярной и ковалентной неполярной связью являются соответственно пары веществ
1) вода и сероводород
2) бромид калия и азот
3) аммиак и водород
4) оксид калия и кислород
5) метан и водород
Ответ: ![]()
11. Ковалентная полярная связь характерна для
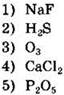
Ответ: ![]()
12. Водородная связь образуется между молекулами
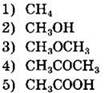
Ответ: ![]()
13. Наиболее прочная химическая связь имеет место в молекуле
1) F2 .
2) Сl2 .
3) O2
4) N2
Ответ: ![]()
14. В молекуле какого вещества длина связи между атомами углерода наибольшая?
1) ацетилена
2) этана
3) этена
4) бензола
Ответ: ![]()
15. Степень окисления, равную +6, атом хрома имеет в соединениях
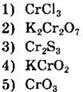
Ответ: ![]()
16. Степень окисления углерода в СН3Сl равна
1) +1
2) -1
3) +2
4) -2
Ответ: ![]()
17. Степень окисления +3 фосфор имеет в соединениях

Ответ: ![]()
18. Высшую степень окисления сера проявляет в соединениях

Ответ: ![]()
19. Молекулярную кристаллическую решетку имеет
1) нитрат калия
2) оксид кремния
3) хлороводород
4) оксид фосфора(V)
5) хлорид бария
Ответ: ![]()
20. Какие из приведенных утверждений верны?
А. Вещества с молекулярной решеткой имеют низкие температуры плавления и низкую электропроводность.
Б. Вещества с атомной решеткой пластичны и обладают высокой электрической проводимостью.
1) верно только А.
2) верно только Б
3) верны оба утверждени.
4) оба утверждения неверны
Ответ: ![]()
21. Молекулярная кристаллическая решетка характерна для
1) хлорида калия
2) брома
3) алюминия
4) сероводорода
5) сульфата натрия
Ответ: ![]()
22. К окислительно-восстановительным реакциям не относят разложение
1) метана
2) азотной кислоты
3) хлорида аммония
4) гидроксида цинка
5) нитрата аммония
Ответ: ![]()
23. С наибольшей скоростью водород реагирует с
1) бромом .
2) иодом
3) фтором .
4) хлором
Ответ: ![]()
24. Химическое равновесие в системе
![]()
сместится в сторону обратной реакции, если
1) повысить давление
2) добавить катализатор
3) уменьшить концентрацию Н2
4) повысить температуру
5) увеличить концентрацию С4Н6
Ответ: ![]()
25. В каком из растворов с одинаковой концентрацией содержание ионов РО43- наибольшее?
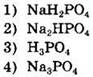
Ответ: ![]()
26. Реакция ионного обмена между растворами сульфата алюминия и хлорида бария протекает до конца в результате взаимодействия ионов:
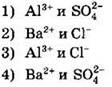
Ответ: ![]()
27. Углерод является окислителем в реакциях с
1) водой
2) алюминием
3) оксидом меди(II)
4) серной кислотой
5) водородом
Ответ: ![]()
28. Установите соответствие между уравнением реакции и формулой вещества, которое в данной реакции является окислителем.
|
УРАВНЕНИЕ РЕАКЦИИ
|
ОКИСЛИТЕЛЬ
|
|
A |
Б |
В |
Г |
29. Установите соответствие между формулой соли и продуктом, который образуется на инертном аноде при электролизе ее водного раствора.
|
ФОРМУЛА СОЛИ
|
ПРОДУКТ НА АНОДЕ 1) водород 2) кислород 3) металл 4) хлор 5) сера 6) азот |
|
A |
Б |
В |
Г |
30. Необратимыми являются реакции, схемы которых
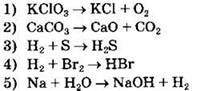
Ответ: ![]()
31. Oт увеличения площади поверхности соприкосновения реагентов не зависит скорость реакций между
1) бензолом и хлором
2) кремнием и кислородом
3) водородом и кислородом
4) цинком и соляной кислотой
5) серой и железом
Ответ: ![]()
32. Химическое равновесие в системе
![]()
смещается в сторону исходных веществ в результате
1) увеличения концентрации водорода
2) повышения температуры
3) уменьшения концентрации бутана
4) использования катализатора
5) повышения давления
Ответ: ![]()
33. Диссоциация ортофосфорной кислоты по второй ступени происходит в соответствии с уравнением
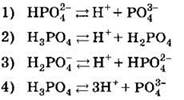
Ответ: ![]()
34. Осадок образуется при взаимодействии растворов сульфата калия и
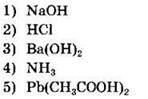
Ответ: ![]()
35. Восстановителем в реакции
![]()
является
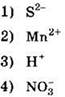
Ответ: ![]()
36. Одинаковую реакцию среды имеют растворы карбоната натрия и
1) нитрата бария
2) силиката калия
3) фосфата натрия
4) сульфата цинка
5) хлорида алюминия
Ответ: ![]()
37. Нейтральную среду имеют водные растворы
1) нитрата калия
2) силиката натрия
3) сульфата лития
4) нитрита калия
5) хлорида железа(II)
Ответ: ![]()
38. Реакции нейтрализации соответствуют уравнения реакций:
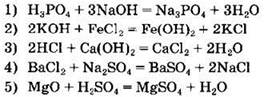
Ответ: ![]()
39. Скорость реакции между железом и раствором серной кислоты будет уменьшаться при
1) повышении температуры
2) разбавлении кислоты
3) увеличении концентрации кислоты
4) измельчении железа
Ответ: ![]()
40. Химическое равновесие в системе
![]()
смещается вправо при
1) повышении давления
2) повышении концентрации СO2
3) понижении температуры
4) повышении температуры
Ответ: ![]()
41. Наибольшее количество нитрат-ионов образуется в растворе при диссоциации 1 моль
1) нитрата алюминия
2) нитрата меди(II)
3) нитрата натрия
4) нитрата кальция
5) нитрата железа(III)
Ответ: ![]()
42. Сокращенное ионное уравнение
![]()
соответствует взаимодействиям
1) свинца и серной кислоты
2) оксида свинца и сульфата калия
3) нитрата свинца(II) и сульфата натрия
4) ацетата свинца(II) и серной кислоты
5) гидроксида свинца(II) и сульфата бария
Ответ: ![]()
43. Окислительно-восстановительными не являются реакции
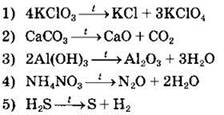
Ответ: ![]()
44. Одинаковую реакцию среды имеют растворы хлорида калия и
1) нитрата алюминия
2) хлорида цинка
3) сульфата железа(II)
4) нитрата натрия
5) бромата калия
Ответ: ![]()
45. Установите соответствие между схемой реакции и формулой недостающего в ней азотсодержащего продукта реакции.
|
СХЕМА РЕАКЦИИ
|
ФОРМУЛА ВЕЩЕСТВА
|
|
А |
Б |
В |
Г |
46. Установите соответствие между уравнением окислительно-восстановительной реакции и изменением степени окисления серы в ней.
|
УРАВНЕНИЕ РЕАКЦИИ
|
ИЗМЕНЕНИЕ СТЕПЕНИ ОКИСЛЕНИЯ СЕРЫ 1) от -2 до +4 2) от -2 до 0 3) от 0 до -2 4) от +6 до +4 5) от +4 до +6 |
|
А |
Б |
В |
Г |
47. Установите соответствие между схемой реакции и формулой недостающего в ней вещества.
|
СХЕМА РЕАКЦИИ
|
ФОРМУЛА ВЕЩЕСТВА
|
|
A |
Б |
В |
Г |
48. Установите соответствие между схемой химической реакции и изменением степени окисления восстановителя.
|
СХЕМА РЕАКЦИИ
|
ИЗМЕНЕНИЕ СТЕПЕНИ ОКИСЛЕНИЯ ВОССТАНОВИТЕЛЯ
|
|
А |
Б |
В |
Г |
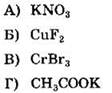
49. Установите соответствие между формулой соли и отношением этой соли к гидролизу.
|
ФОРМУЛА СОЛИ
|
ОТНОШЕНИЕ К ГИДРОЛИЗУ 1) гидролизуется по катиону 2) гидролизуется по аниону 3) гидролизуется по катиону 4) и аниону не гидролизуется |
|
А |
Б |
В |
Г |
50. Установите соответствие между названием соли и ее отношением к гидролизу.
|
НАЗВАНИЕ СОЛИ А) хлорид калия Б) фосфат натрия В) сульфид магния Г) нитрат алюминия |
ОТНОШЕНИЕ К ГИДРОЛИЗУ 1) гидролизуется по катиону 2) гидролизуется по аниону 3) гидролизуется по катиону 4) и аниону не гидролизуется |
|
А |
Б |
В |
Г |
51. Установите соответствие между названием соли и отношением ее к гидролизу.
|
НАЗВАНИЕ СОЛИ А) нитрат калия Б) сульфид бария В) хлорид алюминия Г) карбонат натрия |
ОТНОШЕНИЕ К ГИДРОЛИЗУ 1) гидролизуется по катиону 2) гидролизуется по аниону 3) гидролизуется по катиону 4) и аниону не гидролизуется |
|
А |
Б |
В |
Г |
52. Установите соответствие между названием соли и отношением ее к гидролизу.
|
НАЗВАНИЕ СОЛИ А) хлорид цинка Б) сульфид калия В) нитрат кальция Г) нитрат меди(II) |
ОТНОШЕНИЕ К ГИДРОЛИЗУ 1) гидролизуется по катиону 2) гидролизуется по аниону 3) гидролизуется по катиону 4) и аниону не гидролизуется |
|
А |
Б |
В |
Г |
53. Установите соответствие между формулой соли и продуктом, образующимся на инертном аноде при электролизе ее водного раствора.
|
ФОРМУЛА СОЛИ
|
ПРОДУКТ НА АНОДЕ
|
|
А |
Б |
В |
Г |
54. Установите соответствие между формулой соли и продуктом, образующимся на катоде при электролизе ее водного раствора.
|
ФОРМУЛА СОЛИ
|
ПРОДУКТ НА АНОДЕ
|
|
А |
Б |
В |
Г |
55. Установите соответствие между формулой соли и продуктами электролиза ее водного раствора, которые выделились на инертных электродах: к каждой позиции, данной в первом столбце, подберите соответствующую позицию из второго столбца.
|
ФОРМУЛА СОЛИ
|
ПРОДУКТ ЭЛЕКТРОЛИЗА
|
|
A |
Б |
В |
Г |
56. Используя метод электронного баланса, составьте уравнение реакции:
![]()
Определите окислитель и восстановитель.
57. Используя метод электронного баланса, составьте уравнение реакции:
![]()
Определите окислитель и восстановитель.
58. Используя метод электронного баланса, составьте уравнение реакции:
![]()
Определите окислитель и восстановитель.
59. Используя метод электронного баланса, составьте уравнение реакции:
![]()
Определите окислитель и восстановитель.
60. Используя метод электронного баланса, составьте уравнение реакции:
![]()
Определите окислитель и восстановитель.