Химия самостоятельная подготовка к ЕГЭ - универсальные материалы с методическими рекомендациями, решениями и ответами - 2018 год
Ароматические углеводороды (арены) - Теоретический материал - ОРГАНИЧЕСКАЯ ХИМИЯ
По химическим свойствам арены отличаются от предельных и непредельных углеводородов. Это объясняется особенностями строения бензольного кольца. Делокализация шести π-электронов в циклической системе понижает энергию молекулы, что обусловливает повышенную устойчивость (ароматичность) бензола и его гомологов.
Поэтому арены не склонны вступать в реакции присоединения или окисления, которые ведут к нарушению ароматичности.
Для аренов более характерны реакции, идущие с сохранением ароматической системы, а именно реакции замещения атомов водорода, связанных с циклом.
Другие реакции (присоединение, окисление), в которых участвуют делокализованные углерод-углеродные связи бензольного кольца и нарушается его ароматичность, идут с трудом.
1. Реакции замещения
а) Галогенирование
Замещение атома водорода в бензольном кольце на галоген происходит в присутствии катализаторов АlСl3, АlВr3, FeCl3 и т.п. (кислот Льюиса):

б) Нитрование
Бензол реагирует с нитрующей смесью (смесью концентрированных азотной и серной кислот):
![]()
Гомологи бензола (алкилбензолы) более активно вступают в реакции замещения по сравнению с бензолом.
Например, при нитровании толуола С6Н5СН3 может происходить замещение не одного, а трех атомов водорода с образованием 2,4,6-тринитротолуола:
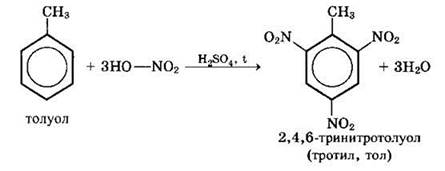
в) Алкилирование
Замещение атома водорода в бензольном кольце на алкильную группу (алкилирование) происходит под действием алкилгалогенидов (реакция Фриделя-Крафтса) или алкенов в присутствии катализаторов АlСl3, АlВr3, FeCl3.
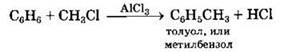
г) Алкилирование бензола алкенами
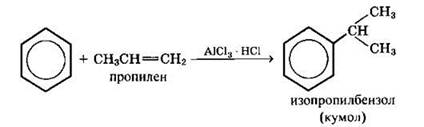
2. Присоединение
В реакции присоединения, приводящие к разрушению ароматической структуры бензольного кольца, арены могут вступать с большим трудом.
а) Гидрирование
Присоединение водорода к бензолу и его гомологам происходит при повышенной температуре и давлении в присутствии металлических катализаторов.
Гидрирование бензола и его гомологов:
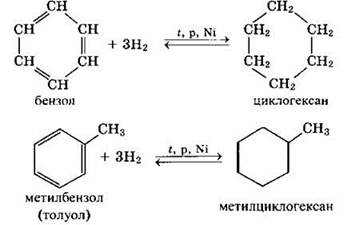
Эта реакция является обратной образованию бензола при дегидрировании циклогексана.
б) Хлорирование (радикальный механизм)
В условиях радикальных реакций (ультрафиолетовое облучение) возможно присоединение галогенов к ароматическим соединениям.
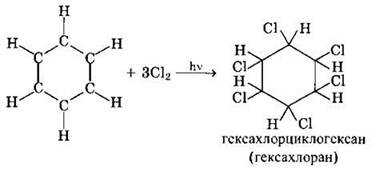
Заметим, что в случае гомологов бензола более легко происходит реакция радикального замещения атомов водорода в боковой цепи:
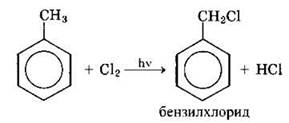
3. Окисление
Бензол не окисляется даже под действием сильных окислителей (КМnO4, К2Сr2O7 и т.п.). Поэтому он часто используется как инертный растворитель при проведении реакций окисления других органических соединений. В отличие от бензола его гомологи окисляются довольно легко.
При действии раствора КМnO4 в кислой среде и нагревании в гомологах бензола окислению подвергаются только боковые цепи:
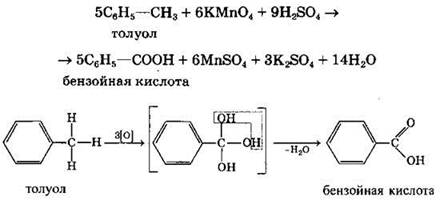
Окисление других гомологов (этилбензол, пропилбензол и т.д.) также приводит к образованию бензойной кислоты. Разрыв связи при этом происходит между двумя ближайшими к кольцу атомами углерода в боковой цепи.
Например:
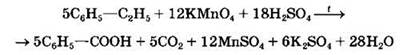
Алкильные группы в алкилбензолах окисляются легче, чем сами алканы. Это объясняется влиянием бензольного кольца на атомы в боковой цепи.
Одно из производных ароматических углеводородов — стирол (винилбензол) также окисляется перманганатом калия в кислой среде:
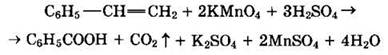
Бензол и его гомологи на воздухе горят коптящим пламенем, что обусловлено высоким содержанием углерода в их молекулах:
![]()
Бензол и его летучие гомологи образуют с воздухом и кислородом взрывоопасные смеси.
1 Электрофильное присоединение — это процесс присоединения частицы, несущей положительный заряд (Н+; NO2+ и т.д.), к фрагменту молекулы, имеющей частично отрицательный заряд.