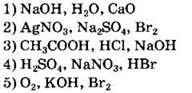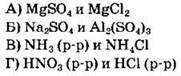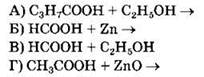Химия самостоятельная подготовка к ЕГЭ - универсальные материалы с методическими рекомендациями, решениями и ответами - 2018 год
ВАРИАНТ 3 - ПРИМЕРНЫЕ ВАРИАНТЫ ЕГЭ
Часть 1
Ответами к заданиям 1-23 является последовательность цифр. Запишите ответ в поле ответа в тексте работы, а затем перенесите в БЛАНК ОТВЕТОВ № 1 справа от номера соответствующего задания, начиная с первой клеточки. Последовательность цифр записывайте без пробелов, запятых и других дополнительных символов. Каждый символ пишите в отдельной клеточке в соответствии с приведенными в бланке образцами.
1. Неспаренные электроны в основном состоянии присутствуют в частицах
1) Mg .
2) F .
3) S
4) Ne
5) Р3-
Ответ: ![]()
2. В периоде с увеличением порядкового номера элемента уменьшается
1) атомный радиус
2) кислотность соответствующих оксидов
3) электроотрицательность элементов
4) неметаллические свойства простых веществ
5) основность гидроксидов
Ответ: ![]()
3. Одна из связей, образованная по донорно-акцепторному механизму, присутствует в
1) Н2O2
2) HNO3
3) СО
4) СO2
5) СаО
Ответ: ![]()
4. Одинаковую степень окисления азот проявляет в веществах, формулы которых
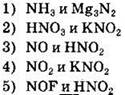
Ответ: ![]()
5. Молекулярное строение имеют

Ответ: ![]()
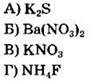
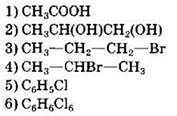
6. Выберите формулы трех веществ, относящихся к классу кислот, и запишите соответствующие им номера в ячейки ответа

Ответ: ![]()
7. Как сера, так и калий реагируют с
1) алюминием
2) оксидом углерода(II)
3) водородом
4) оксидом натрия
5) азотной кислотой
Ответ: ![]()
8. Оксид цинка реагирует с
1) оксидом натрия
2) оксидом углерода(IV)
3) углеродом
4) серебром
5) азотом
Ответ: ![]()
9. Гидроксид калия реагирует с каждым из двух веществ:
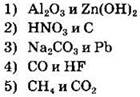
Ответ: ![]()
10. Гидрокарбонат калия можно перевести в карбонат калия действием

Ответ: ![]()
11. В заданной схеме превращений
![]()
веществами X и Y являются:

Ответ: ![]()
12. Изомером гексена-2 являются
1) 2,3-диметилпентен-1
2) 2,3-диметилбутадиен-1,3
3) 3-метилпентин-1
4) 1,3-диметилциклобутан
5) 3-метилпентен-2
Ответ: ![]()
13. С аммиачным раствором оксида серебра реагирует
1) бутин-1 .
2) бутин-2 .
3) бутадиен-1,2
4) изопрен
5) ацетилен
Ответ: ![]()
14. С пропанолом-1 реагирует каждое из двух веществ:
1) бутен и изобутан
2) пропин и этен
3) натрий и бромоводород
4) ацетилен и железо
5) оксид меди(II) и этаналь
Ответ: ![]()
15. И с гидроксидом меди(II), и с гидрокарбонатом натрия реагирует
1) С2Н5ОН
2) НСООН
3) С2Н5—О—С2Н5
4) С2Н5—СООН
5) НО—СН2—СН2—ОН
Ответ: ![]()
16. Этанол можно получить в результате реакции
1) окисления этаналя
2) гидратации этена
3) гидролиза этилацетата
4) гидрирования этилена
5) окисления этана
Ответ: ![]()
17. Аланин в отличие от уксусной кислоты реагирует с
1) гидроксидом кальция
2) натрием
3) хлороводородом
4) аммиаком
5) серной кислотой
Ответ: ![]()
18. В заданной схеме превращений
![]()
веществами X и Y являются:
1) хлорэтан
2) этилен
3) 1-хлорбутан
4) метилпропан
5) 2-хлорбутан
Ответ: ![]()
19. Из предложенного перечня выберите две характеристики реакции взаимодействия железа с хлоридом меди(II).
1) каталитическая
2) обратимая
3) эндотермическая
4) окислительно-восстановительная
5) замещения
Ответ: ![]()
20. Из приведенного списка выберите схему реакции, протекающей при обычных условиях наиболее быстро (А) и наиболее медленно (Б).
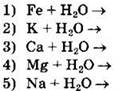
Ответ: 
21. К слабым электролитам относится каждое из двух веществ
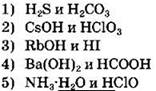
Ответ: ![]()
22. Растворы сахарозы и глюкозы можно отличить с помощью

Ответ: ![]()
23. В присутствии катализатора в промышленности осуществляют
1) синтез хлороводорода
2) синтез аммиака
3) алкилирование аренов
4) ректификацию сырой нефти
5) поглощение оксида серы(VI)
Ответ: ![]()
Ответом к заданиям 24-26 является число. Запишите это число в поле ответа в тексте работы, соблюдая при этом указанную степень точности. Затем перенесите это число в БЛАНК ОТВЕТОВ № 1 справа от номера соответствующего задания, начиная с первой клеточки. Каждый символ пишите в отдельной клеточке в соответствии с приведенными в бланке образцами. Единицы измерения физических величин писать не нужно._
24. В 200 г 8%-ного раствора нитрата калия добавили 10 соли и 40 г воды. Чему равна массовая доля соли в полученном растворе?
Ответ:________ % (запишите число с точностью до десятых).
25. В результате реакции, термохимическое уравнение которой:
![]()
выделилось 66,6 кДж теплоты. Масса использованного алюминия составила _________ г. (Запишите ответ с точностью до сотых).
26. Вычислите массу кислорода, необходимого для полного сжигания 4,4 г пропана.
Ответ: ________ г (запишите число с точностью до целых).
В заданиях 27-35 к каждому элементу первого столбца подберите соответствующий элемент из второго столбца и запишите в таблицу выбранные цифры под соответствующими буквами. Получившуюся последовательность цифр перенесите в БЛАНК ОТВЕТОВ № 1 без пробелов, запятых и других дополнительных символов. Цифры в ответе могут повторяться..
27. Установите соответствие между названием вещества и общей формулой класса, к которому это вещество принадлежит.
|
НАЗВАНИЕ ВЕЩЕСТВА |
ОБЩАЯ ФОРМУЛА |
|
А) изобутан |
|
|
Б) дивинил |
|
|
В) этин |
|
|
Г) 2,3-диметилгексан |
|
Ответ: 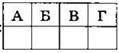
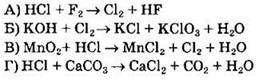
28. Установите соответствие между схемой реакции и свойством хлора, которое этот элемент проявляет в данной реакции.
|
СХЕМА РЕАКЦИИ |
СВОЙСТВО ХЛОРА 1) только окислитель 2) только восстановитель 3) и окислитель, и восстановитель 4) ни окислитель, ни восстановитель |
|
|
Ответ: 
29. Установите соответствие между формулой соли и продуктом, выделяющимся на аноде в ходе электролиза водного раствора этой соли.
|
ФОРМУЛА СОЛИ |
ПРОДУКТ НА АНОДЕ 1) фтор 2) кислород 3) бром 4) азот 5) сернистый газ 6) водород |
|
|
Ответ: 
30. Установите соответствие между формулой соли и отношением ее к гидролизу.
|
ФОРМУЛА СОЛИ |
ОТНОШЕНИЕ К ГИДРОЛИЗУ 1) гидролизуется по катиону 2) гидролизуется по аниону 3) гидролизуется по катиону и по аниону 4) не гидролизуется |
|
|
Ответ: 
31. Установите соответствие между способом воздействия на равновесную систему
![]()
и направлением смещения химического равновесия в результате этого воздействия:
|
ВОЗДЕЙСТВИЕ НА СИСТЕМУ A) уменьшение давления Б) добавление катализатора B) увеличение температуры Г) уменьшение концентрации кислорода |
НАПРАВЛЕНИЕ СМЕЩЕНИЯ ХИМИЧЕСКОГО РАВНОВЕСИЯ 1) в сторону продуктов реакции 2) в сторону исходных веществ 3) практически не смещается |
Ответ: 
32. Установите соответствие между формулой вещества и реагентами, с каждым из которых это вещество может реагировать.
|
ФОРМУЛА ВЕЩЕСТВА |
РЕАГЕНТЫ
|
|
|
Ответ: 
33. Установите соответствие между формулами веществ и реактивом, позволяющим их различить.
|
ВЕЩЕСТВА |
РЕАКТИВ
|
|
|
Ответ: 
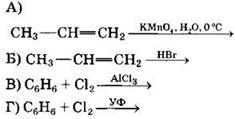
34. Установите соответствие между схемой реакции и формулой органического продукта, преимущественно образующегося в ходе реакции.
|
СХЕМА РЕАКЦИИ |
ФОРМУЛА ПРОДУКТА |
|
|
Ответ: 
35. Установите соответствие между схемой реакции и названием органического продукта, преимущественно образующегося в ходе реакции.
|
СХЕМА РЕАКЦИИ |
НАЗВАНИЕ ПРОДУКТА 1) формиат цинка 2) этилформиат 3) ацетат цинка 4) пропионат цинка 5) этилбутират 6) метилацетат |
|
|
Ответ: 
Часть 2
Для записи ответов на задания 36-40 используйте БЛАНК ОТВЕТОВ № 2. Запишите сначала номер задания (36, 37 и т.д.), а затем его подробное решение. Ответы записывайте четко и разборчиво.
36. Используя метод электронного баланса, составьте уравнение реакции
![]()
Определите окислитель и восстановитель.
37. Аммиак окислили кислородом в присутствии платины как катализатора. Полученное при этом вещество прореагировало с кислородом, при этом образовался бурый газ. Газ поглотили раствором гидроксида натрия. Одно из полученных при этом веществ прореагировало с раствором, содержащим перманганат калия и гидроксид калия. Напишите уравнения четырех описанных реакций.
38. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
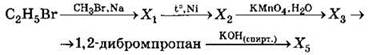
При написании уравнений реакций используйте структурные формулы органических веществ.
39. Навеска смеси двух солей — гидросульфата натрия и сульфата натрия с массовой долей сульфата в ней 60% — может вступить в реакцию с 70 мл 10%-го раствора гидроксида натрия (ρ = 1,11 г/мл). На такую же навеску подействовали избытком раствора гидроксида стронция. Найдите массу осадка, образовавшегося при этом.
40. При сгорании 11,6 г органического вещества образуется 13,44 л углекислого газа и 10,8 г воды. Плотность паров этого вещества по воздуху равна 2. Установлено, что это вещество взаимодействует с аммиачным раствором оксида серебра, каталитически восстанавливается водородом с образованием первичного спирта и способно окисляться подкисленным раствором перманганата калия до карбоновой кислоты. На основании этих данных:
1) произведите вычисления, необходимые для установления молекулярной формулы органического вещества;
2) запишите молекулярную формулу исходного органического вещества;
3) составьте структурную формулу этого вещества, которая однозначно отражает порядок связи атомов в его молекуле;
4) приведите уравнение реакции его взаимодействия с водородом.