Химия ОГЭ - Основной государственный экзамен - Комплекс материалов для подготовки учащихся - Д.Ю. Добротин - 2018 год
ВАРИАНТ 10 - ПРИМЕРНЫЕ ВАРИАНТЫ ОГЭ 2017
Часть 1
При выполнении заданий 1—15 в поле ответа запишите одну цифру, которая соответствует номеру правильного ответа.
1. На приведённом рисунке

изображена модель атома
1) хлора
2) фосфора
3) фтора
4) кремния
Ответ: [ ]
2. Электроотрицательность фосфора меньше, чем электроотрицательность
1) кремния
2) азота
3) алюминия
4) магния
Ответ: [ ]
3. Такой же вид химической связи, как и в молекуле ССl4, характерен для
1) РН3
2) NaCl
3) MgO
4) CaBr2
Ответ: [ ]
4. Степень окисления хлора в Mg(BrO3)2равна
1) +2
2) +3
3) -1 .
4) +5
Ответ: [ ]
5. Вещества, формулы которых H2SO4 и Сl2O7, являются соответственно
1) солью и основным оксидом
2) кислотой и амфотерным оксидом
3) кислотой и кислотным оксидом
4) солью и кислотой
Ответ: [ ]
6. Образование новых веществ происходит при
1) горении нефти
2) испарении бензина
3) замерзании воды
4) нагревании речного песка
Ответ: [ ]
7. 3 моль катионов образуется при полной диссоциации 1 моль
1) фосфата калия
2) нитрата железа(III)
3) хлорида алюминия
4) азотной кислоты
Ответ: [ ]
8. Сокращённое ионное уравнение ![]() соответствует взаимодействию веществ
соответствует взаимодействию веществ

Ответ: [ ]
9. С водородом реагирует
1) аммиак
2) гидроксид натрия
3) сера
4) фосфорная кислота
Ответ: [ ]
10. Оксид алюминия реагирует с
1) соляной кислотой
2) водой
3) кислородом
4) гидроксидом железа(II)
Ответ: [ ]
11. И соляная кислота, и гидроксид калия взаимодействуют с

Ответ: [ ]
12. Среди веществ: СаСО3, Ва(NО3)2, CuSO4, - в реакцию с соляной кислотой вступает(-ют)
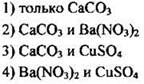
Ответ: [ ]
13. Верны ли суждения о правилах работы в химической лаборатории?
А. Запрещается герметично закрывать колбу во время нагревания в ней жидкости.
Б. Получение хлора всегда проводят в вытяжном шкафу.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
Ответ: [ ]
14. В реакции, схема которой
![]()
окислителем является
![]()
Ответ: [ ]
15. На какой диаграмме распределение массовых долей элементов соответствует количественному составу сульфата лития?

Ответ: [ ]
При выполнении заданий 16, 17 из предложенного перечня ответов выберите два правильных и запишите в таблицу цифры, под которыми они указаны.
16. В ряду химических элементов: Li → Be → В
1) уменьшается число протонов в ядрах атомов
2) уменьшается электроотрицательность
3) увеличивается число электронов во внешнем электронном слое атомов
4) уменьшается степень окисления в высших оксидах
5) усиливаются кислотные свойства высших оксидов
Ответ: ![]()
17. Для глицерина верны следующие утверждения:
1) молекула содержит 3 атома кислорода
2) является газообразным веществом (н.у.)
3) атомы углерода в молекуле соединены с атомами кислорода двойной связью
4) характерны реакции присоединения
5) вступает в реакцию с натрием
Ответ: ![]()
При выполнении заданий 18, 19 к каждому элементу первого столбца подберите соответствующий элемент из второго столбца. Запишите в таблицу выбранные цифры под соответствующими буквами. Цифры в ответе могут повторяться.
18. Установите соответствие между реагирующими веществами и признаком протекающей между ними реакции.
|
РЕАГИРУЮЩИЕ ВЕЩЕСТВА |
ПРИЗНАК РЕАКЦИИ |
|
|
1) выпадение белого осадка |
|
2) выпадение жёлтого осадка |
|
|
3) выпадение голубого осадка 4) выпадение серо-зелёного осадка |
Ответ:
|
А |
Б |
В |
19. Установите соответствие между формулой вещества и реагентами, с каждым из которых оно может взаимодействовать.
|
ФОРМУЛА ВЕЩЕСТВА
|
РЕАГЕНТЫ
|
|
Ответ:
|
А |
Б |
В |
Часть 2
Для ответов на задания 20-22 используйте отдельный лист. Запишите сначала номер задания (20, 21 или 22), а затем развёрнутый ответ к нему, Ответы записывайте чётко и разборчиво.
20. Используя метод электронного баланса, составьте уравнение реакции
![]()
Определите окислитель и восстановитель.
21. Оксид меди(II) массой 32 г может прореагировать с 146 г раствора соляной кислоты. Определите массовую долю кислоты в растворе.
22. Для проведения эксперимента предложены следующие реактивы: Са(ОН)2(тв); растворы: СаСl2, Ba(NO3)2, HNO3, НСl, Na2CO3
Используя воду и необходимые вещества только из этого списка, получите в две стадии нитрат кальция. Напишите уравнения реакций. Опишите признаки проводимых реакций. Для второй реакции напишите сокращённое ионное уравнение.