Химия - Новый полный справочник для подготовки к ОГЭ - 2018 год
Кислородсодержащие вещества: спирты (метанол, этанол, глицерин), карбоновые кислоты (уксусная и стеариновая) - Первоначальные сведения об органических веществах
Спирты
Спиртами называются органические соединения, в молекулах которых углеводородный радикал соединён с одной или несколькими гидроксогруппами, например:
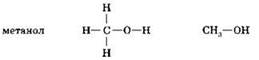
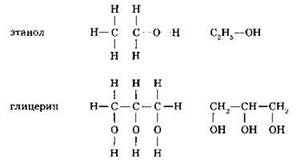
Метанол (метиловый спирт) и этанол (этиловый спирт) относятся к одноатомным спиртам, т.к. их молекулы содержат одну гидроксогруппу. Глицерин относится к многоатомным спиртам, т.к. его молекула содержит три гидроксогруппы.
Метанол и этанол представляют собой бесцветные легко кипящие жидкости с характерным запахом, смешиваются с водой в любых соотношениях. Метанол (древесный спирт) чрезвычайно ядовит, небольшое количество его приводит к потере зрения и даже к смертельному исходу. В промышленности метанол получают из оксида углерода(Ii) и водорода:
![]()
Этиловый спирт получают различными способами, например — сбраживанием сахаристых веществ или гидратацией этилена:
![]()
Все спирты — вещества горючие, при их сгорании на воздухе выделяется большое количество теплоты:
![]()
При нагревании с водоотнимающими средствами спирты могут вступать в реакции дегидратации (отщепления воды). В случае этанола в ходе дегидратации могут образоваться или диэтиловый эфир, или этилен:
![]()
Метанол и этанол взаимодействуют с щелочными металлами с выделением водорода и с образованием солеобразных продуктов — алкоголятов:
![]()
В этой реакции спирты проявляют кислотные свойства.
Спирты могут также взаимодействовать с галогеноводородными кислотами, например:
![]()
В ходе этой реакции происходит замещение гидроксогруппы в молекуле спирта на атом галогена. Подобная реакция напоминает взаимодействие оснований с кислотами, что может указывать на основные свойства спиртов. С учётом предыдущей реакции можно говорить о химической двойственности спиртов.
Многоатомные спирты имеют свои особенности. Так, глицерин представляет собой очень вязкую сиропообразную жидкость с характерным сладким вкусом, хорошо растворяющуюся в воде. Характерным свойством глицерина является его способность растворять свежеосаждённый гидроксид меди(II) с образованием ярко-синего раствора (качественная реакция на многоатомные спирты). При взаимодействии глицерина с азотной кислотой образуется нитроглицерин:
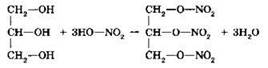
Метанол применяется в качестве растворителя, добавки к автомобильному топливу, в химической промышленности для производства пластмасс, уксусной кислоты и др. Этанол используют как сырьё в органическом синтезе, в качестве растворителя, а также в качестве сырья в пищевой промышленности. Глицерин используется для приготовления антифризов (незамерзающих жидкостей), в кожевенной, пищевой, фармацевтической промышленности. На основе нитроглицерина готовят взрывчатые вещества (динамит) и лекарственные препараты.
Карбоновые кислоты
Карбоновыми кислотами называют органические вещества, молекулы которых содержат карбоксильную группу —СООН.
Простейшими карбоновыми кислотами являются муравьиная и уксусная:

К карбоновым относятся и другие известные вам органические кислоты, например лимонная или щавелевая:
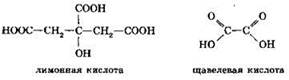
Если муравьиная и уксусная кислоты — летучие жидкости с резким и неприятным запахом, то лимонная и щавелевая кислоты — вещества кристаллические, без запаха. В воде все эти кислоты хорошо растворимы. Водный раствор уксусной кислоты с содержанием её 3-9% называют столовым уксусом, с содержанием 70% — уксусной эссенцией. Уксусная кислота используется в пищевой и химической промышленности.
При большом числе атомов углерода в молекулах кислот их относят к высшим карбоновым кислотам. Одной из высших карбоновых кислот является стеариновая кислота С17Н35—СООН. Стеариновая кислота — вещество твёрдое, без запаха, цвета и вкуса, в воде нерастворима. В промышленности получается гидролизом жиров.
По химическим свойствам карбоновые кислоты напоминают кислоты минеральные (неорганические). И те и другие изменяют окраску индикаторов, реагируют с металлами, основаниями, основными оксидами. Вот несколько типичных уравнений реакций с участием карбоновых кислот.
1. Диссоциация в водном растворе:
![]()
Знак обратимости указывает на слабые кислотные свойства карбоновых кислот. Так, укусная кислота слабее сернистой, азотистой, фтороводородной кислот, но сильнее таких кислот, как сероводородная или угольная.
2. Реакция нейтрализации:
![]()
В ходе реакции нейтрализации образуется соль и вода. Соли уксусной кислоты называются ацетатами, соли муравьиной кислоты — формиатами, соли стеариновой кислоты — стеаратами. Натриевые и калиевые соли стеариновой кислоты составляют основу мыла. Поскольку кислотные свойства карбоновых кислот слабы, их соли в водных растворах подвергаются гидролизу, обуславливая щелочную среду раствора, например:
![]()
или в ионном виде:
![]()
3. Взаимодействие с металлами:
![]()
Поскольку карбоновые кислоты относятся к слабым кислотам, то они могут взаимодействовать только с активными и средней активности металлами.
4. Взаимодействие с основными оксидами:
![]()
5. Взаимодействие с солями:
![]()
Эта реакция возможна, т.к. в ходе её уксусная кислота выделяет более слабую угольную из её соли (угольная кислота сразу же распадается на углекислый газ и воду).
В химии карбоновых кислот важное место занимает реакция этерификации — взаимодействие со спиртами, приводящее к получению сложных эфиров. Подробнее о протекании этой реакции вы узнаете в старших классах.
Задания
Часть 1
К каждому из заданий части 1 даны 4 варианта ответа, из которых только один правильный.
1. Формула метанола
1) CH3OH
3) HCOOH
2) НСНО
4) СН3СН2ОН
2. Формула этанола
1) СН3ОН
3) НСООН
2) НСНО
4) СН3СН2ОН
3. К спиртам относятся все вещества в группе
1) СН3СООН, СН3ОН, C2H5OH
2) С2Н5ОН, С3Н7ОН, СН3ОН
3) НСНО, СН3ОН, С2Н5ОН
4) СН3СНО, СН3ОН, НСНО
4. В состав карбоновых кислот входит функциональная группа
1) —ОН
2) —СООН
3) —СНО .
4) —СН3
5. Уксусная кислота не взаимодействует с
1) оксидом кальция
2) гидроксидом натрия
3) оксидом серы(IV)
4) карбонатом натрия
6. Какие связи образует атом кислорода в молекуле метанола?
1) одну σ-связь
2) две σ-связи
3) одну σ- и одну π-связи
4) две π-связи
7. Какие связи образует атом углерода в молекуле муравьиной кислоты?
1) одну σ-связь
2) две σ-связи
3) одну σ- и одну π-связи
4) три σ- и одну π-связи
8. Свежеприготовленный осадок Сu(ОН)2 растворится, если к нему добавить
1) глицерин.
2) этанол
3) метанол .
4) этилен
9. Характерной реакцией для многоатомных спиртов является их взаимодействие с
1) Н2O .
2) Сu
3) Вr2 .
4) Сu(ОН)2
10. При взаимодействии муравьиной кислоты с магнием образуются
1) формиат магния и вода
2) формиат магния и водород
3) ацетат магния и вода
4) ацетат магния и водород
11. При взаимодействии уксусной кислоты с цинком образуются
1) формиат цинка и вода
2) формиат цинка и водород
3) ацетат цинка и вода
4) ацетат цинка и водород
12. При взаимодействии уксусной кислоты с оксидом цинка образуются
1) формиат цинка и вода
2) формиат цинка и водород
3) ацетат цинка и вода
4) ацетат цинка и водород
13. Уксусная кислота не взаимодействует с веществом, формула которого
1) Са
2) Са(OН)2.
3) Сu
4) NaOH
14. Этанол можно получить из этилена в результате реакции
1) гидратации
2) гидрирования
3) галогенирования
4) гидрогалогенирования
15. Глицерин в водном растворе можно определить с помощью
1) бромной воды
2) нитрата серебра
3) гидроксида меди(II)
4) гидроксида натрия